
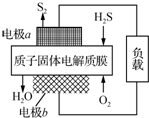
 H2S������Դ������;��֮һ�ǻ����������õ�������Ӧԭ��Ϊ��2H2S��g��+O2��g���TS2��s��+2H2O��l����H=-632kJ•mol-1����ͼΪ����ĤH2Sȼ�ϵ�ص�ʾ��ͼ������˵����ȷ���ǣ�������
H2S������Դ������;��֮һ�ǻ����������õ�������Ӧԭ��Ϊ��2H2S��g��+O2��g���TS2��s��+2H2O��l����H=-632kJ•mol-1����ͼΪ����ĤH2Sȼ�ϵ�ص�ʾ��ͼ������˵����ȷ���ǣ�������| A�� | �缫aΪ��ص����� | |
| B�� | �缫b�Ϸ����ĵ缫��ӦΪ��O2+2H2O+4e-�T4OH- | |
| C�� | ��·��ÿ����4 mol���ӣ�����ڲ��ͷ�632 kJ���� | |
| D�� | ÿ34 g H2S���뷴Ӧ����2 mol H+������Ĥ���������� |
���� ����2H2S��g��+O2��g���TS2��s��+2H2O��Ӧ���ó�����H2Sʧ���ӷ���������Ӧ������O2�õ��ӷ�����ԭ��Ӧ���ݴ˷������
��� �⣺A����2H2S��g��+O2��g���TS2��s��+2H2O��Ӧ���ó�����H2Sʧ���ӷ���������Ӧ����aΪ��صĸ�������A����
B������O2�õ��ӷ�����ԭ��Ӧ�����Ե缫b�Ϸ����ĵ缫��ӦΪ��O2+4H++4e-=2H2O����B����
C����·��ÿ����4mol���ӣ�������1mol����������װ�ý���ѧ��ת��Ϊ���ܣ����Ե���ڲ��������ų���������C����
D��ÿ34g��1molH2S���뷴Ӧ��������0.5mol�����������O2+4H++4e-=2H2O��������2molH+������Ĥ��������������D��ȷ��
��ѡD��
���� ������ؿ���ԭ���ԭ������ȷ�������Һ������ǽⱾ��ؼ����ѵ��ǵ缫��Ӧʽ����д����Ŀ�ѶȲ���


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʵ����� | ����ͽ��� | |
| A | ��ƽ��3KSCN+FeCl3?Fe��SCN��3+3KCl����Һ�м�������KCl��Һ | ��Һ��ɫ��dz��ƽ�������ƶ� |
| B | ��AgI�����е���KCl��Һ | �а�ɫ�����ɣ�Ksp��AgCl����Ksp��AgI�� |
| C | ��Cl2ͨ��Ʒ����Һ�� | ��Һ��ɫ��Cl2����Ư���� |
| D | ��Fe��NO3��2��Һ�е��������ữ��H2O2��Һ | ��Һ��Ϊ��ɫ�������ԣ�H2O2��Fe3+ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Ӽ����������Ǽ��Լ� | B�� | ��������Լ����Ǽ��Լ� | ||
| C�� | ��������Լ������Ӽ������� | D�� | ���Ӽ���������������Ǽ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
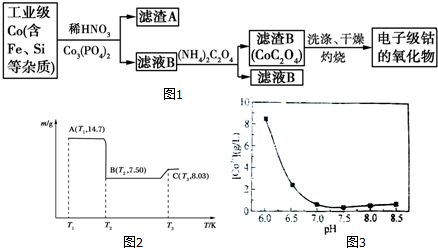
| ��ʼ������pH | ��ȫ������pH | |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Co2+ | 7.2 | 9.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ�е�Ԫ�ر����� | |
| B�� | �÷�Ӧ��H2O2����ԭ�� | |
| C�� | ʵ��������NaCN��Һʱ�������������NaOH��Һ | |
| D�� | �����£�Ũ�Ⱦ�Ϊ0.1 mol•L-1 NaCN��NaHCO3��Һ��ǰ�ߵ�pHС�ں��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
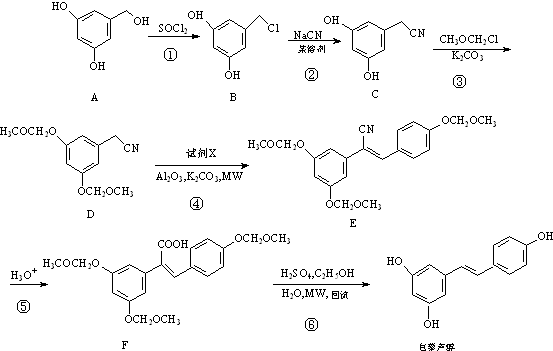
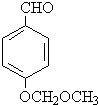 ��
��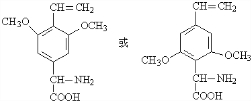 ��
��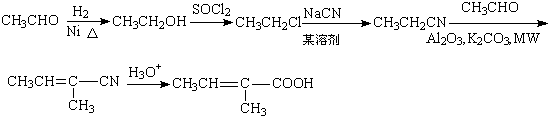 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | N O P | B�� | Li Be Mg | C�� | C N P | D�� | Ar Cl F |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Na2S2O3��Һ��ͨ������������S2O32-+2Cl2+3H2O�T2SO32-+4Cl-+6H+ | |
| B�� | ���������Ũ�ȵ�Ba��OH��2ϡ��Һ��NH4HCO3ϡ��Һ��ϣ�Ba2++2OH-+NH4++HCO3-�TBaCO3��+NH3•H2O+H2O | |
| C�� | ����������Һ��̼����þ��Һ��Ӧ��HCO3-+Ca2++OH-�TCaCO3��+H2O | |
| D�� | ��ǿ����Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��3ClO-+2Fe��OH��3�T2FeO42-+3Cl-+H2O+4H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Һ��ɫ���ֲ��䣬˵���������淴Ӧ�ﵽƽ��״̬ | |
| B�� | �����̷���FeS04•7H2O������ԭ��������1 L��ˮ��������Ҫ458.7g | |
| C�� | ������ת����Ӧ��ƽ�ⳣ��K=1��1014����ת����������Һ��pH=5 | |
| D�� | ������Ksp=1��10-32��Ҫʹ�������ˮ�е�c��Cr3+������1��10-5mol/L��Ӧ����Һ��pH=5 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com