
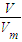 各组分气体的物质的量,再根据m=nM计算各组分质量并求和.
各组分气体的物质的量,再根据m=nM计算各组分质量并求和.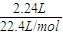 ×44g/mol+
×44g/mol+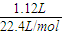 ×32g/mol=6.0g,
×32g/mol=6.0g,

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案科目:高中化学 来源: 题型:
A.1∶1∶1 B.1∶1∶
查看答案和解析>>
科目:高中化学 来源: 题型:
①1∶1∶1 ②1∶1∶2 ③2∶2∶3 ④1∶2∶3
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,将4.48 L SO2、CO2、H2的混合气,通入适量饱和NaHCO3溶液中,充分反应后溶液中的溶质只有NaHSO3,而且逸出的气体只有CO2和H2,其质量之和为4.6 g,则原混合气中SO2、CO2、H2的体积之比可能是( )
A.1∶1∶1 B.1∶1∶2 C.2∶1∶1 D.1∶2∶3
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.6.0 g | B.4.8 g | C.3.2 g | D.5.6 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com