
| 组分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数/% | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
分析 I.(1)用氧化物的形式表示其组成,书写顺序是:活泼金属元素氧化物、较活泼金属元素氧化物、二氧化硅、水;
(2)AlFe(OH)nCl6-n中各元素的化合价代数和为0;
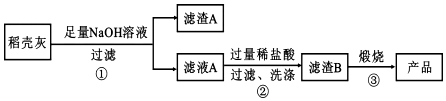
II.稻壳灰用足量的氢氧化钠浸泡,过滤得A为硅酸钠溶液,滤渣A含有C以及氧化铁,硅酸钠溶液中加入盐酸生成硅酸沉淀,过滤、洗涤得滤渣B为硅酸,煅烧硅酸可得二氧化硅,以此解答该题.
解答 解:I.(1)石棉(CaMg3Si4O12)是常用的耐火材料,用氧化物的形式表示其组成,书写顺序是:活泼金属元素氧化物、较活泼金属元素氧化物、二氧化硅、水,所以为CaO•3MgO•4SiO2,
故答案为:CaO•3MgO•4SiO2;
(2)化合物中铝元素显+3价,氢氧根为-1价,各元素的化合价代数和为0,故铁元素的化合价为+3价;
故答案为:+3;
II.稻壳灰用足量的氢氧化钠浸泡,过滤得A为硅酸钠溶液,滤渣A含有C以及氧化铁,硅酸钠溶液中加入盐酸生成硅酸沉淀,过滤、洗涤得滤渣B为硅酸,煅烧硅酸可得二氧化硅,
(1)二氧化硅为酸性氧化物,氧化钠、氧化铁为碱性氧化物,氧化铝为两性氧化物,故答案为:Al2O3;
(2)二氧化硅为酸性氧化物,与氢氧化钠反应生成硅酸钠和水,离子方程式:SiO2+2OH-=SiO32-+H2O;
故答案为:SiO2+2OH-═SiO32-+H2O;
(3)氧化钠、氧化钾均能与水反应生成可溶性碱,氧化铝为两性氧化物能够与强碱反应生成可溶性偏铝酸盐,二氧化硅 为酸性氧化物与氢氧化钠反应生成可溶性硅酸钠,三氧化二铁、碳与氢氧化钠不反应,所以过滤剩余的滤渣为C和Fe2O3;
故答案为:C和Fe2O3.
点评 本题以硅及其化合物性质为载体考查物质的制备以及分离提纯,侧重于学生分析、实验能力的考查,解答本题时注意熟悉氧化物的分类,明确硅及其化合物性质,题目难度中等.


科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫化钠的水解反应:S2-+H3O+?HS-+H2O | |
| B. | 室温下,氯化铵溶液显酸性的理由:NH4++H2O═NH3•H2O+H+ | |
| C. | 泡沫灭火器的反应原理:Al3++3HCO3-═3CO2↑+Al(OH)3↓ | |
| D. | 用铜作电极电解饱和食盐水:2Cl-+H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
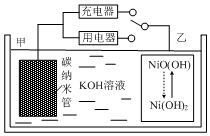 2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )
2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏落户.用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示.下列说法正确的是( )| A. | 放电时,甲电极为正极,OH-移向乙电极 | |
| B. | 放电时,乙电极反应为:Ni(OH)2+OH--e-=NiO(OH)+H2O | |
| C. | 充电时,电池的碳电极与直流电源的正极相连 | |
| D. | 电池总反应为H2+2NiOOH$?_{充电}^{放电}$2Ni(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原电池的正极材料必须是金属 | |
| B. | 原电池的负极发生还原反应 | |
| C. | 实验室欲快速制取氢气,可利用粗锌与稀硫酸反应 | |
| D. | 原电池可以把物质内部的能量全部转化为电能 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可以利用铝热反应冶炼高熔点的金属 | |
| B. | 现代石油化工,采作银作催化剂可以实现一步完成乙烯转化为环氧乙烷的过程,该反应的原子利用率为100% | |
| C. | 工业上制溴是向酸化的浓缩海水中直接通入氯气置换出溴即可 | |
| D. | 煤直接液化可得液体燃料 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 锡青铜的熔点比纯铜高 | |
| B. | 在自然环境中,锡青铜中的锡可对铜起保护作用 | |
| C. | 锡青铜文物在潮湿环境中的腐蚀比干燥环境中快 | |
| D. | 生成Cu2(OH)3Cl覆盖物是电化学腐蚀过程,但不是化学反应过程 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2溶于水产生O2:Na2O2+H2O=2Na++2OH-+O2↑ | |
| B. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| C. | 次氯酸钙溶液中通入过量二氧化碳:Ca2++2ClO-+H2O+CO2=CaCO3↓+2HClO | |
| D. | 将一定量的Al片投入足量的NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com