
【题目】下列各组元素中,都属于短周期主族元素的是
A.Na、ArB.Si、BrC.H、SD.Al、Fe
科目:高中化学 来源: 题型:
【题目】向某NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同,若向溶液M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图所示。则下列分析与判断不正确的是(不计CO2溶解)
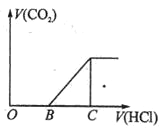
A. 若OB=0,则形成溶液的过程中所发生反应的离子方程式为OH―+CO2═HCO3―
B. 若OB=BC,则溶液M为Na2CO3溶液
C. 若OB>BC,则溶液M中大量存在的阴离子为CO32―和HCO3―
D. 若3OB=BC,则溶液M中c(NaHCO3)=2c(Na2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为分离废磷酸亚铁锂电池的正极材料(主要含LiFePO4和铝箔)中的金属,将正极材料粉碎后进行如下流程所示的转化:

已知LiFePO4不溶于水和碱,能溶于强酸。
(1)“碱溶”时的离子方程式为___。
(2)向滤液Ⅰ中通入过量CO2会析出Al(OH)3沉淀,写出该反应的离子方程式:____。
(3)“酸浸”时溶液中Fe2+发生反应的离子方程式为_____。
(4)检验“沉铁”后所得溶液中是否存在Fe3+的方法是____。
(5)以Fe(OH)3为原料可以制取FeSO4晶体,还需的试剂有____。
(6)“沉锂”时,检验Li+是否沉淀完全的方法是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确且能达到相应目的的是
选项 | 实验目的 | 实验操作 |
A | 称取2.0gNaOH固体 | 先在托盘上各放1张滤纸,然后在右盘上添加2g砝码,左盘上添加NaOH固体 |
B | 配制稀硫酸 | 先将浓硫酸加入烧杯,后倒入蒸馏水 |
C | 验证铁的吸氧腐蚀 | 将铁钉放入试管中,用盐酸浸没 |
D | 检验溶液中是否有NH4+ | 取少量试液于试管中,加入NaOH溶液并加热,用湿润的红色石蕊试纸检验产生的气体 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解质溶液的叙述正确的是
A. 室温下,同浓度的Na2CO3与NaHCO3溶液相比,Na2CO3溶液的pH大
B. 将pH=3的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C. 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同
D. 室温下,pH=7的NH4Cl与氨水的混合溶液中离子浓度大小顺序为:c(Cl-)>c(NH4+)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家最近发现两种粒子:第一种是由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”;第二种是由四个氧原子构成的分子。下列有关这两种粒子的说法正确的是
A. “四中子”的粒子不显电性 B. “四中子”的电子数为4
C. 第二种粒子是氧元素的另一种同位素 D. 第二种粒子是一种化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】只用溴水就可以将下列物质鉴别出来的是
A.水、CCl4、酒精、苯
B.NaCl溶液、NaBr溶液、NaI溶液、NaOH溶液
C.AgNO3溶液、NaOH溶液、KI溶液、CCl4
D.CCl4、酒精、NaCl溶液、KI-淀粉溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(CN)2、(OCN)2、(SCN)2等通称为拟卤素,它们的性质与卤素相似,氧化性强弱顺序是:F2>(OCN)2>Cl2>(CN)2>(SCN)2>I2下列方程式中错误的是( )
A.2NaSCN+MnO2+2H2SO4=Na2SO4+(SCN)2↑+MnSO4+2H2O
B.(CN)2+2KI=2KCN+I2
C.Cl2+2NaOCN=(OCN)2+2NaCl
D.2AgCN=2Ag+(CN)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化铈(CeO2)是一种重要的稀土氧化物,平板电视显示屏生产过程中产生大量的废玻璃粉末(含SiO2、Fe2O3、CeO2、FeO等物质)。某课题组以此粉末为原料,设计如下工艺流程对资源进行回收,得到纯净的CeO2和硫酸铁铵晶体。

已知:CeO2不溶于稀硫酸,也不溶于NaOH溶液。
回答下列问题:
(1)稀酸A的分子式是_____________________________________________。
(2)滤液1中加入H2O2溶液的目的是___________________________________________。
(3)设计实验证明滤液1中含有Fe2+___________________________________________。
(4)在酸性溶液中,已知Fe2+溶液可以和难溶于水的FeO(OH)反应生成Fe3O4,书写该反应的离子方程式____________________________________________________________。
(5)由滤液2生成Ce(OH)4的离子方程式_____________________________________。
(6)硫酸铁铵晶体[Fe2(SO4)3·2(NH4)2SO4·3H2O]广泛用于水的净化处理,但其在去除酸性废水中的悬浮物时效率降低,其原因是__________________________________________。
(7)取上述流程中得到的Ce(OH)4产品0.531 g,加硫酸溶解后,用浓度为0.l000 mol·L-1的FeSO 4标准溶液滴定至终点时(铈被还原为Ce3+ ),消耗25.00 mL标准溶液。该产品中Ce(OH)4的质量分数为______________ (结果保留两位有效数字),Mr(Ce)=140。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com