
【题目】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4+ + 6HCHO = 3H++ 6H2O + (CH2)6N4H+ [滴定时,1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸。某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数 (填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积 (填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察 。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由 色变成 色。
(2)滴定结果如下表所示:

若NaOH标准溶液的浓度为0.1010 mol/L,则该样品中氮元素的质量分数为 。(结果保留四位有效数字)
【答案】(1)①偏高。②无影响。③B。④无;粉红(或浅红)。(2)18.75%。
【解析】
试题分析:(1)①碱式滴定管用蒸馏水洗涤后,没有用NaOH标准溶液润洗就直接加入NaOH标准溶液,使滴定的氢氧化钠溶液的浓度偏小,则消耗氢氧化钠标准溶液体积判断,得测得样品中(CH2)6N4H+偏多,因此结果氮的质量分数偏高;
②锥形瓶用蒸馏水洗涤后,水未倒尽,由于溶液中含有的被程度的物质的物质的量不变,则滴定时用去NaOH标准溶液的体积也不变,因此不会产生任何影响;
③滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶内溶液颜色的变化,故选项B正确;
④由于指示剂酚酞在酸溶液中,用已知浓度的碱滴定未知浓度的酸,因此开始溶液是无色,当滴定达到终点时,酚酞指示剂由无色变成浅红色;
(2)根据实验可知第一次实验反应消耗标准溶液的体积21.03mL-1.02mL=20.01mL;第二次实验反应消耗标准溶液的体积21.99mL-2.00mL=19.99ml;第三次实验反应消耗标准溶液的体积20.20mL-0.20mL=20.00ml;因此反应消耗标准溶液的体积是V=(20.01mL+19.99ml+20.00ml)÷3=20.00mL,根据酸、碱发生中和反应时的物质的量关系是1:1可知:c×25.00mL=0.1010 mol·L-1×20.00mL,解得c=0.0808mol/L,则250mL溶液中含有(CH2)6N4H+及H+的物质的量是0.0808mol/L×0.25L=0.0202mol,则在1.500 g样品中含NH4+的物质的量是0.0202mol,其中含有N的质量是m(N)=0.0202mol×14g/mol=0.2828g,所以N元素的质量分数是(0.2828g÷1.500 g)×100%=18.85%。


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】下图是中学教材中元素周期表的一部分,其中标出A-Q14种元素,试回答下列问题:[(1) (2)问用具体的元素符号或离子符号或化学式回答]
A | B | C | D | ||||||||||||||
E | F | G | H | I | J | K | L | ||||||||||
P | Q |
(1)在上表所列出的短周期元素中
①性质最不活泼的是_______;②原子半径最大的是_____(除稀有气体元素)
③形成的气态氢化物最稳定的是_______;
④最高价氧化物对应的水化物中酸性最强的是_______碱性最强的是_______。
⑤形成的阴离子还原性最弱的是_______,阳离子半径最小的是_______。
(2)用电子式表示F与D形成化合物的过程
________________________________________________________________________;
(3)设P的原子序数为Z,则F的原子序数为___________,Q的原子序数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明氢氟酸是弱酸的实验事实是
A.HF溶液与Zn反应放出H2
B.0.1mol/LNaF溶液的pH大于7[
C.HF溶液与Na2CO3反应生成CO2
D.0.1mol/LHF溶液可使紫色石蕊变红
查看答案和解析>>
科目:高中化学 来源: 题型:
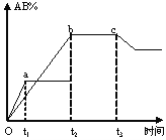
【题目】反应A2+B2 ![]() 2AB在不同条件下,产物AB百分含量随时间变化关系如图所示,a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是( )
2AB在不同条件下,产物AB百分含量随时间变化关系如图所示,a为500℃,b为300℃时情况,c为300℃时从时间t3开始向容器中加压的情况,则下列叙述正确的是( )
A.AB为固体,A2、B2中最少有一种为非气体,正反应吸热
B.AB为气体,A2、B2中最少有一种为非气体,正反应吸热
C.AB为气体,A2、B2中最少有一种为非气体,正反应放热
D.A2、B2、AB均为气体,正反应放热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸钴是制作氧化钴和金属钴的原料。一种利用含钴废料(主要成分Co2O3),含少量Fe2O3、MnO2、Al2O3、CaO、MgO、碳及有机物等)制取草酸钴(CoC2O3)的工艺流程如下:
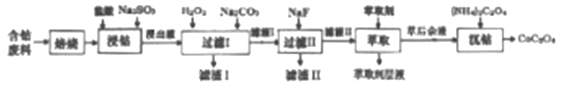
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等。
②部分阳离子一氢氧化物形式沉淀时溶液的pH见下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
完全沉淀时的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
③Kap(MgF2)=7.35×10-11,Kap(CaF2)=1.05×10-10
回答下列问题:
(1)焙烧的目的是_________;浸钴过程中Co3+转化为Co2+,反应的离子方程式为_____________。
(2)加入H2O2的目的是__________,加入Na2CO3溶液,调pH至5.2,滤渣Ⅰ主要成分为__________。
(3)加入过量NaF溶液,可将Ca2+、Mg2+除去,若所得滤液中c(Ca2+)=1.0×10-5mol·L-1,则滤液中c(Mg2+)为_______________。
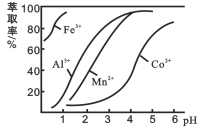
(4)萃取剂对金属离子的萃取率与pH的关系如下图所示。滤液Ⅱ中加入萃取剂的作用是_________;萃取时,溶液的pH需要控制在一定范围内才比较适宜,其pH范围约为__________。
(5)已知含钴废料中含Co2O3质量分数为a%,若取mg该含钴废料按照上述流程,理论上最多能制得CoC2O4的质量为__________g(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(12分)粗食盐常含有少量K+、Ca2+、Mg2+、Fe3+、SO![]() 等杂质离子,实验室提纯NaCl的流程如下:
等杂质离子,实验室提纯NaCl的流程如下:
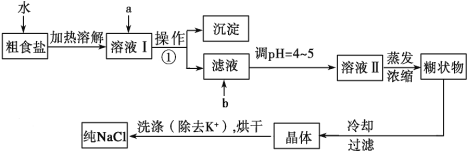
提供的试剂:饱和Na2CO3溶液、饱和K2CO3溶液、NaOH溶液、BaCl2溶液、Ba(NO3)2溶液、75%乙醇、四氯化碳、稀盐酸。
(1)欲除去溶液Ⅰ中的Ca2+、Mg2+、Fe3+、SO![]() ,选出a所代表的试剂,按滴加顺序依次为____________________ (只填化学式)。
,选出a所代表的试剂,按滴加顺序依次为____________________ (只填化学式)。
(2)如何检验 SO![]() 是否沉淀完全 。
是否沉淀完全 。
(3)调节pH 的目的 ,试剂b是 (填名称)。
(4)洗涤除去NaCl晶体表面附带的少量KCl,选用的试剂为_________,使用该试剂的目的是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com