
现有四种元素的基态原子的电子排布式如下:
① 1s22s22p63s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.第一电离能:③>①>②
B.原子半径:③>②>①
C.电负性:③>①>②
D.最高正化合价:③>②>①
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
一定温度下,密闭容器中M、N、R三种气体的初始浓度和平衡浓度如下表所示:
| 物质 | M | N | R |
| 初始浓度/mol•L—1 | 0.20 | 0.30 | 0 |
| 平衡浓度/mol•L—1 | 0.02 | 0.21 | 0.18 |
(1)请通过计算写出此反应的化学方程式。
(2)达平衡时,N的转化率是多少?
(3)该温度下的平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:4NH3(g)+5O2(g)  4NO(g)+6H2O(g),ΔH=-1025kJ·mol-1,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是
4NO(g)+6H2O(g),ΔH=-1025kJ·mol-1,该反应是一个可逆反应。若反应物起始物质的量相同,下列关于该反应的示意图不正确的是

查看答案和解析>>
科目:高中化学 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。

请回答:
(1)B极是电源的 极, 丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明 在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比依次为 。
(3)现用丙装置给铜件镀银,则H应该是 (填“镀层金属”或“镀件”),电镀液是 溶液。当乙中溶液的pH是13时(此时乙溶液体积为500mL),丙中镀件上析出银的质量为 ,甲中溶液的pH (填“变大”、“变小”或“不变”)。
(4)乙中发生总反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列现象与氢键有关的是
①H2O的熔、沸点比VIA族其他元素氢化物的高 ②小分子的醇、羧酸可以和水以任意比互溶 ③冰的密度比液态水的密度小 ④NH3在水中的溶解度很大 ⑤邻羟基苯甲酸的熔、沸点比对羟基苯甲酸的低 ⑥水分子高温下也很稳定:
A.①②③④⑤⑥ B. ①②③④⑤
C. ①②③④ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表述不正确的是
A.福岛核电站泄露的放射性物质131I与127I互为同位素,化学性质几乎相同
B.电子云是处于一定空间运动状态的电子在原子核外空间的概率密度分布的形象化描述
C.凡是中心原子采取sp3杂化方式成键的分子其几何构型都是正四面体
D.钠原子L层共有8种运动状态不同的电子
查看答案和解析>>
科目:高中化学 来源: 题型:
氮元素可以形成多种化合物。回答以下问题:
(1)C、N、O三种元素第一电离能从大到小的顺序是____________。
(2)N≡N的键能为942 kJ·mol-1,N-N单键的键能为247 kJ·mol-1。计算说明N2中的
键更稳定(填“p”或“σ”)。
(3)已知CN-与N2结构相似,推算HCN分子中σ键与p键数目之比为 ;
N2与O22+互为等电子体,O22+的电子式可表示为 。
(4)肼(N2H4)分子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一
种氮的氢化物。
①NH3分子的空间构型是_____________;N2H4分子结构式为_________。
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2 N2H4 (l)===3N2(g)+4H2O(g) △H=-1038.7kJ·mol-1
若该反应中有4mol N-H键断裂,则形成的p键有________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列混合溶液中,各离子浓度的大小顺序正确的是( )
A. 10 mL 0.1 mol ·L-1氨水与10 mL 0.1 mol ·L-1盐酸混合,
c(Cl-)>c(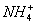 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B. 10 mL 0.1 mol ·L-1NH4Cl溶液与5 mL 0.2 mol ·L-1NaOH溶液混合,
c(Na+)=c(Cl-)>c(OH-)>c(H+)
C. 10 mL 0.1 mol ·L-1CH3COOH溶液与5 mL 0.2 mol ·L-1NaOH溶液混合,
c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D. 10 mL 0.5 mol ·L-1CH3COONa溶液与6 mL 1 mol ·L-1盐酸混合,
c(Cl-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
用98%的浓硫酸(密度1.84g · mL-1)配制100mL 1mol·L-1的稀硫酸。现给出下列配制 中可能用到的仪器:①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平
⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒。按使用仪器的先后顺序作出的下列排列中正
确的是( )
A.④③⑥⑦⑤⑥ B.②⑥③⑦⑤⑥ C.①③⑤⑦⑤⑥ D.②③⑥⑦⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com