
分析 (1)根据胶体和溶液的区别,胶体的颗粒直径为1-100 nm,溶液的颗粒直径为1 nm,胶体有丁达尔现象,不能透过半透膜,强电解质会破坏胶体的稳定性,形成沉淀等知识点;
(2)豆浆具有胶体的性质.
解答 解:(1)A.氯化铁溶液属于溶液,颗粒直径小于1 nm,故A错误;
B.氢氧化铁胶体颗粒直径为1-100 nm,不能透过半透膜,故B错误;
C.氯化铁加入氢氧化钠溶液反应生成氢氧化铁红褐色沉淀,氢氧化铁胶体加入浓氢氧化钠溶液后胶粒发生团聚,形成氢氧化铁沉淀,为红褐色,故C正确;
D.氯化铁为黄褐色溶液,故D错误,
故答案为:C;
(2)豆浆具有胶体的性质,向其中加入盐卤,盐卤中含丰富的电解质氯化钙等,可以使豆浆凝聚,故答案为:用盐卤点豆腐.
点评 本题考查胶体的性质以及胶体和溶液的区别,题目难度不大,注意氯化铁溶液是黄色的液体,氢氧化铁胶体是红褐色液体,D为易错点.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:选择题
| A. | H+ | B. | SO42- | C. | OH- | D. | Na+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeO | B. | Fe2O3 | C. | FeCl3 | D. | Fe3O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 0.012kg12C含有约6.02×1023个碳原子 | |
| C. | 1个氧原子的实际质量约为$\frac{6.02×1{0}^{23}}{32}$g | |
| D. | 3molOH-的质量为51g |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
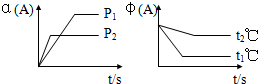
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学平衡是动态平衡 | |
| B. | 各反应物的浓度等于各生成物的浓度 | |
| C. | 正逆反应速率为零 | |
| D. | 反应物和生成物的浓度不再改变,反应已停止 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素相对原子质量依次递增 | |
| B. | 元素的最高正化合价呈周期性变化 | |
| C. | 元素原子最外层电子排布呈周期性变化 | |
| D. | 元素金属性或非金属性呈周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴离子的半径:Z>Y | |
| B. | 气态氢化物稳定性:Z>Y>X | |
| C. | 氧化物的水化物的酸性:Z>Y | |
| D. | 元素W、X、Z各自最高和最低化合价的代数和分别为0、2、6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com