
分析 KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O中,I元素的化合价由+5价降低为0,I元素的化合价由-1价升高为0,该反应中转移5e-,结合淀粉遇碘单质变蓝来解答.
解答 解:(1)KIO3中I元素的化合价降低,则KIO3为氧化剂,故答案为:KIO3;
(2)氧化还原反应KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O中,化合价升高值=化合价降低值=转移电子数=5e-,用双线桥表示该反应电子转移的方向和数目为: ,故答案为:
,故答案为: ;
;
(3)在上述反应中,转移5mol电子生成碘单质的量是3mol,所以如果反应中转移0.2mol电子,则生成I2的物质的量为0.2mol×$\frac{3}{5}$=0.12moL,故答案为:0.12mol;
(4)食盐中加碘加的是碘酸钾,可以将碘酸根离子转化为碘单质,需要一种还原剂(碘化钾)来实现,再根据碘单质遇到淀粉显示蓝色来检验,在酸性环境下,碘酸根离子和碘离子之间反应生成碘单质,所以选择的试剂有:KI溶液、淀粉溶液、稀硫酸,
故答案为:②③④.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意电子转移的计算及表示方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Mg原子的电子式 Mg: | B. | 二氧化硅的结构式O=Si=O | ||
| C. | 14O的原子结构示意图  | D. | 氯化钠的分子式 NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4Cl 与 ZnCl2溶液可作焊接金属中的除锈剂 | |
| B. | 用 NaHSO4去除暖手瓶中的水垢 | |
| C. | 实验室盛放 Na2CO3溶液的试剂瓶不能用磨口玻璃塞 | |
| D. | 加热蒸干 AlCl3溶液得到 Al(OH)3固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去乙醇中少量的水:加足量生石灰,蒸馏 | |
| B. | 分离苯和硝基苯的混合物,可用蒸馏法 | |
| C. | 可用苯将溴从溴苯中萃取出来 | |
| D. | 可用水来鉴别苯、乙醇、四氯化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | (b-2a)/3mol•L-1 | B. | (b-2a)/2mol•L-1 | C. | (2b-a)/3mol•L-1 | D. | (2b-a)/2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与浓硝酸、浓硫酸共热并保持55~60℃可反应生成硝基苯 | |
| B. | 甲苯与氯气在光照下发生一元取代反应,主要生成2-氯甲苯或4-氯甲苯 | |
| C. | 乙苯可被酸性高锰酸钾溶液氧化为 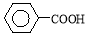 (苯甲酸) (苯甲酸) | |
| D. | 苯乙烯在合适条件下催化加氢可生成乙基环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量的H2O与D2O含有的中子数 | |
| B. | 等质量的SO2和SO3中含有氧原子数 | |
| C. | 同温同压下,同体积的CO和NO含有的质子数 | |
| D. | 等物质的量的铁和铝分别于足量氯气完全反应时转移的电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10g H2和10g O2 | B. | 5.6LCCl4(标准状况)和11gCO2 | ||
| C. | 9gH2O和0.5molBr2 | D. | 224mL H2(标准状况)和0.1molN2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
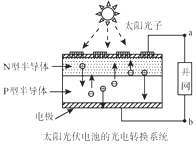 世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最.下列有关叙述正确的是( )
世博会中国馆、主题馆等建筑所使用的光伏电池,总功率达4兆瓦,是历届世博会之最.下列有关叙述正确的是( )| A. | 电流从a流向b | |
| B. | N型半导体为正极,P型半导体为负极 | |
| C. | 光伏电池是将化学能转变为电能 | |
| D. | 光伏电池是将太阳能转变为电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com