
【题目】“玉兔”号月球车用 ![]() Pu作为热源材料.下列关于
Pu作为热源材料.下列关于 ![]() Pu的说法正确的是( )
Pu的说法正确的是( )
A.![]() Pu与
Pu与 ![]() U互为同位素
U互为同位素
B.![]() Pu与
Pu与 ![]() Pu互为同素异形体
Pu互为同素异形体
C.![]() Pu与
Pu与 ![]() U具有完全相同的化学性质
U具有完全相同的化学性质
D.![]() Pu与
Pu与 ![]() Pu具有相同的最外层电子数
Pu具有相同的最外层电子数
科目:高中化学 来源: 题型:
【题目】肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g) =N2O4(l) ΔH1=-19.5 kJ·mol-1
②N2H4(l)+O2(g) = N2(g)+2H2O(g) ΔH2=-534.2 kJ·mol-1
(1)写出肼和N2O4反应的热化学方程式______________;
(2)上述反应中氧化剂是______________。
(3)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4 (g) ![]() 2NO2 (g)
2NO2 (g)
① 上述反应的ΔH_________0(选填“>”或“<”)。
② 保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,再次达到平衡时,混合气体中NO2的体积分数_______(填“增大”、“ 减小”或“不变”),混合气体的颜色_______(填“变深”或“变浅”)。
③一定温度下,将1 mol N2O4 充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是___________。
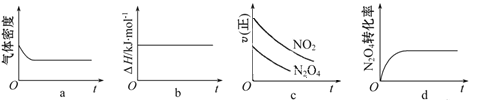
④若在相同温度下,上述反应改在体积为10L的恒容密闭容器中进行,反应3s后NO2的物质的量为0.6mol,则0-3s内的平均反应速率v(N2O4)=___________ mol·L-1·s-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。以卤块为原料可制得轻质氧化镁,工艺流程如图:
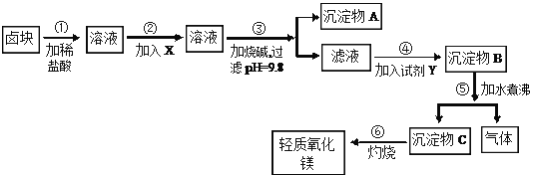
已知:Fe2+氢氧化物呈絮状,不易从溶液中除去,所以常将它氧化为Fe3+,生成Fe(OH)3沉淀除去。若要求产品尽量不含杂质,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH | 表2 化学试剂价格表 | ||||
物质 | 开始沉淀 | 沉淀完全 | 试剂 | 价格(元/吨) | |
Fe(OH)3 | 2.7 | 3.7 | 漂液(含25.2% NaClO) | 450 | |
Fe(OH)2 | 7.6 | 9.6 | 双氧水(含30% H2O2) | 2400 | |
Mn(OH)2 | 8.3 | 9.8 | 烧碱(含98% NaOH) | 2100 | |
Mg(OH)2 | 10.0 | 11.1 | 纯碱(含99.5% Na2CO3) | 600 | |
(1)在步骤②中加入的试剂X(从表2中选择)是_______而不是双氧水,其原因是_______________________。写出加入X发生反应的离子方程式_______________________。
(2)在步骤③中控制pH=9.8,其目的是____________________________。
(3)沉淀物A的成分为______________,试剂Y(从表2中选择)应该是_______。
(4)在步骤⑤中发生反应的化学方程式是________________________。
(5)若在实验室中完成步骤⑥,则沉淀物C必需在_______(填仪器名称)中灼烧。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是
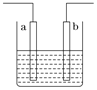
A. a、b不可能是同种材料的电极
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. 该装置可能是原电池,电解质溶液为稀盐酸
D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( ) 
A.最简单气态氢化物的热稳定性:R>Q
B.最高价氧化物对应水化物的酸性:Q<W
C.原子半径:T>Q>R
D.W对应的单质只可以跟强碱反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事故或药品的处理正确的是( )
A.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
B.当出现CO中毒时,应立即将中毒者抬到室外通风处
C.制取并收集氧气结束后,应立即停止加热
D.将含硫酸的废液倒入水槽,用水冲入下水道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备氮化镁的装置示意图如下:

回答下列问题:
(1)检查装置气密性的方法是______________________,a的名称是_____________________。
(2)写出NaNO2和(NH4)2SO4反应制备氮气的化学方程式___________________________________。
(3)C的作用是________________________,D的作用是________________,是否可以把C和D的位置对调并说明理由_________________________________。
(4)写出E中发生反应的化学方程式_____________________________________。
(5)请用化学方法确定是否有氮化镁生成,并检验是否含有未反应的镁,写出实验操作及现象_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CH4催化还原NOx可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g)ΔH=-574 kJ·mol-1
②CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g)ΔH=-1 160 kJ·mol-1
下列说法不正确的是( )
A. 反应①②均为放热反应
B. 等物质的量的甲烷分别发生反应①②,转移电子数相同
C. 由反应①可推知:CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(l) ΔH=-a kJ·mol-1,a<574
D. 若用标准状况下4.48 L CH4还原NO2至N2,放出的热量为173.4 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com