
| A�� | �����Ƽ��ȡ�����Ĺ��չ����о�Ӧ���������ܽ�ȵIJ��� | |
| B�� | ������һ�գ���ˮ�����գ���ȡ֭������������ȡ�����صĹ����з����˻�ѧ�仯 | |
| C�� | �������ѩ��ǿ��֮���������𡱣��ϱ����պ뾰������صļ�����������������ɫ��Ӧ | |
| D�� | ʹ�ÿ�������Դ���ó��ٽ������̼����л��ܼ���ע��ԭ�ӵľ����ԡ����õ��ܺ��������յȶ�����ɫ��ѧ������ |
���� A�������Ƽ����ñ�����Һ��̼�������ܽ��С��������������ȡ���չ����м�NaCl����֬�����ε��ܽ�ȣ�
B����ȡ���������仯��
C����Ԫ�ص���ɫ��ӦΪ��ɫ��
D���ó��ٽ������̼����л��ܼ���������Ⱦ��
��� �⣺A�������Ƽ����ñ�����Һ��̼�������ܽ��С��������������ȡ���չ����м�NaCl����֬�����ε��ܽ�ȣ����Ӧ���������ܽ�ȵIJ��죬��A��ȷ��
B����������ȡ�����صĹ�������������ȡ����ȡ���������仯����B����
C����Ԫ�ص���ɫ��ӦΪ��ɫ����������ػ������ɫ�����Զ�����صļ�����������������ɫ��Ӧ����C��ȷ��
D���ó��ٽ������̼����л��ܼ���������Ⱦ����ע��ԭ�ӵľ����ԡ����õ��ܺ��������յȶ�����ɫ��ѧ�����ݣ���D��ȷ��
��ѡB��
���� ���⿼�����ʵ����ʼ���;��Ϊ��Ƶ���㣬�������ʵ����ʡ������ķ�Ӧ����������;�Ĺ�ϵΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��Ԫ�ػ�����֪ʶ��Ӧ�ã���Ŀ�ѶȲ���


 100�ִ�����ĩ���ϵ�д�
100�ִ�����ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
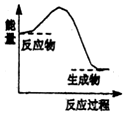
| A�� | ��������������ķ�Ӧ | |
| B�� | ����þ������ķ�Ӧ | |
| C�� | ����������̼���������̼�ķ�Ӧ | |
| D�� | Ba��OH��2•8H2O������NH4Cl����ķ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
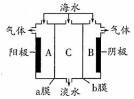 ��ˮ�к��д���Na+��C1-������Ca2+��Mg2+��SO42-���õ��������Ըú�ˮ��Ʒ���е�����������ͼ��ʾ������˵����ȷ���ǣ�������
��ˮ�к��д���Na+��C1-������Ca2+��Mg2+��SO42-���õ��������Ըú�ˮ��Ʒ���е�����������ͼ��ʾ������˵����ȷ���ǣ�������| A�� | bĤ�������ӽ���Ĥ | |
| B�� | A���Ҳ������ݲ����������������� | |
| C�� | ����������ɺ�A��B��C������pH��СΪpHA��pHB��pHC | |
| D�� | B���Ҳ����������ʹʪ���KI������ֽ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| M | N | ||
| X | Y | Z |
| A�� | ����⻯����ȶ��ԣ�M��N��Z | B�� | ��ۺ���������ԣ�Z��M��Y | ||
| C�� | ���ʵ��۵㣺X��Z��N | D�� | �����ӵİ뾶��Z��N��X |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
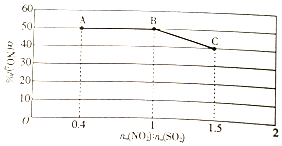 ��֪NO2����SO2�ܷ�����Ӧ��NO2��g��+SO2��g��?SO3��g��+NO��g����
��֪NO2����SO2�ܷ�����Ӧ��NO2��g��+SO2��g��?SO3��g��+NO��g�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ϊ��ʹ�������ۺ��е��ԣ�����ʱ��ʹ�õ��飨����Ư���ԣ����ռ� | |
| B�� | ����Mgʧ��ʱ��������ĭ��������� | |
| C�� | ��������������ɣ��������̬���ʵ����� | |
| D�� | ˮ���������������ϼ��ͷ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
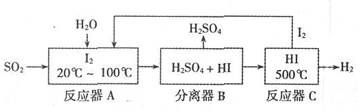
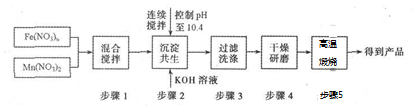
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| ��ѧʽ | AgCl | Ag2CrO4 | CH3COOH | H2CO3 | HClO |
| Ksp��Ka | Ksp=1.8��10-10 | Ksp=2��10-12 | Ka=1.8��10-5 | Ka1=4.3��10-7 Ka2=5.6��10-11 | Ka=3��10-8 |
| A�� | lmolCl2ͨ��������ˮ�г�ַ�Ӧ��ת�Ƶĵ�����ԼΪ6.02��1023 | |
| B�� | ������CO2����ͨ��NaClO��Һ�е����ӷ���ʽ��CO2+H2O+ClO-�THCO3-+HC1O | |
| C�� | �����£�������ˮ����ϡ�ʹ��ᣬ��Һ��$\frac{c��C{H}_{3}COOH��}{c��{H}^{+}��}$��ֵ���� | |
| D�� | ��Ũ�Ⱦ�Ϊ1��103 mol/L-1��KC1��K2CrO4�����Һ�еμ�1��10-3 mol/L-1��AgNO3��ҺCl-�ȳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | E |
| A�� | HnDOmΪǿ��ʱ��E�ķǽ�����һ����ǿ | |
| B�� | A��OH��nΪǿ��ʱ��B��OH��mҲһ��Ϊǿ�� | |
| C�� | EԪ�ص�����ϼ�Ϊ+7ʱ��DԪ�صĸ����ϼۿ�Ϊ-2�� | |
| D�� | HnCOmΪǿ��ʱ��E�ĵ��ʿ�����ǿ��ԭ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com