
【题目】化学与生产、生活、环境保护等密切相关。下列叙述正确的是
A. 为防止或减少酸雨的发生,将含硫废气向高空排放
B. 为防止细菌危害人体健康,常用明矾对饮用水消毒杀菌
C. 为防止电池导致重金属污染,废旧电池应作回收处理
D. 为防止食品受潮变质,可在食品包装袋中放入铁粉
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】实验室使用pH传感器来测定Na2CO3和NaHCO3混合物中NaHCO3的含量.称取1.59g样品,溶于水配成250.00mL溶液,取出该溶液25.00mL用0.1molL﹣1盐酸进行滴定,得到如图曲线.以下说法或操作正确的是( )
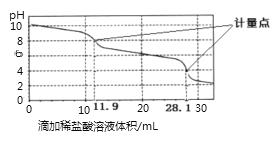
A. 上一个计量点前发生反应的离子方程式为HCO3﹣+H+═H2O+CO2↑
B. 下一个计量点溶液中存在大量的阴离子是Cl﹣、HCO3﹣
C. 此样品n(NaHCO3)=(28.1﹣2×11.9)×10﹣4 mol
D. 使用该方法测定Na2CO3和NaOH混合溶液中的氢氧化钠含量,将会得到1个计量点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中,受热时均易分解。实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如下图所示。
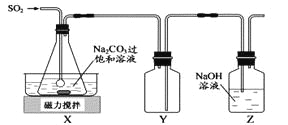
当溶液pH约为4时,停止反应。在20℃静置结晶,生成Na2S2O5的化学方程式为2NaHSO3=2Na2S2O5+H2O。
(1)SO2与Na2CO3溶液反应生成NaHSO3和CO2,其离子方程式为 。
(2)装置Y的作用是 。
(3)析出固体的反应液经减压抽滤,洗涤,25℃-30℃干燥,可获得Na2S2O5固体。
①组成减压抽滤装置的主要仪器是布氏漏斗、 和抽气泵。
②依次用饱和SO2水溶液、无水乙醇洗涤Na2S2O5固体,用饱和SO2水溶液洗涤的目的是 。
(4)实验制得的Na2S2O5固体中含有一定量的Na2SO3和Na2SO4,其可能的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄糖在不同条件下可以被氧化成不同物质。请结合题意回答问题:已知:RCOOH+CH2===CH2+![]() O2
O2![]() RCOOCH===CH2+H2O
RCOOCH===CH2+H2O
(1)葡萄糖在酒化酶作用下生成有机物A,A、B、C、D、E间的转化关系如下图所示:

①B是石油化学工业最重要的基础原料,写出A→B的化学方程式:___________________________________________。
②D的结构简式为_____________________________。
(2)葡萄糖在一定条件下还可氧化为X和Y(Y和A的相对分子质量相同)。X可催化氧化成Y,也可与H2反应生成Z。X和Y的结构中有一种相同的官能团是________,检验此官能团需用的试剂是________。
(3)F是人体肌肉细胞中的葡萄糖在缺氧的条件下进行无氧呼吸的产物。F、G、H间的转化关系是:F![]() G
G![]() H,H与(1)中的D互为同分异构体。
H,H与(1)中的D互为同分异构体。
①G还可以发生的反应有________(填字母)
a.加成反应 b.水解反应 c.氧化反应 d.消去反应 e.还原反应
②本题涉及的所有有机物中,与F不论以何种质量比混合(总质量一定),完全燃烧生成CO2和H2O的物质的量不变的有(写结构简式)______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组以含铁的废铝为原料制备硫酸铝晶体,设计如下的实验方案:

请回答以下问题:
(1)上述实验中多次用到过滤操作,该操作中要用到的玻璃仪器有 ;
(2)步骤②中有洗涤沉淀的操作,如何判断沉淀已洗涤干净: ;
(3)写出步骤②所得沉淀受热分解的化学方程式 ,指出两种产物在物质分类上的类别 、 ;
(4)步骤①中使用的NaOH溶液以4mol/L为宜。某同学称量mgNaOH固体配制V mL 4mol/L的NaOH溶液,下面是该同学配制过程的示意图,其操作中有错误的是(填操作序号) 。

第⑤部操作可能会使所配溶液浓度偏 (填“大”或“小”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下某溶液中由水电离出的H+浓度为1.0×10﹣13molL﹣1,则在此溶液中一定不可能大量存在的离子组是( )
A. Al3+、K+、NO3﹣、Cl﹣ B. K+、Na+、HCO3﹣、Cl﹣
C. Na+、CO32﹣、SO42﹣、NO3﹣ D. Ba2+、Na+、Cl﹣、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常用工业酒精和生石灰混合蒸馏法制取无水乙醇。如图是实验室中模拟工业原理制取无水乙醇的装置。

回答下列问题:
(1)指出图中的几处错误:____________________________。
(2)在除去工业酒精中的水时,下列做法不可取的是____________。
A.加入过量的生石灰后过滤
B.加入过量的生石灰后蒸馏
C.加入过量的生石灰后分液
(3)由(2)可知除去工业酒精中的水的原理是(用化学方程式表示):_____________。
(4)装置中仪器A、B、C的名称分别是:A____________;B_______________;C_____________。
(5)在蒸馏操作中,仪器B中加入沸石(或碎瓷片)的作用是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写下列空白:
(1)有6.02×l023个H的H2O,其物质的量是_______;1molNa2SO4中所含的离子总数目为______。
(2)_____molH2O中含有的氧原子数与1.5molCO2中含有的氧原子数相等。
(3)将等物质的量的NH3和CH4混合,混合气体中NH3与CH4的质量比为_______。
(4)要使NH3与CH4含相同数目的H原子,则NH3和CH4的物质的量之比为________。
(5)标准状况下,密度为0.75g·L-1的NH3与CH4组成的混合气体中,该混合气体对氢气的相对密度为____________。
(6)已知agA和bgB恰好完全反应生成0.2molC和dgD,则C的摩尔质量为_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com