
分析 A与B(卤素)生成的化合物X表示为ABn,X对氢气的相对密度为77,则ABn的相对分子质量为77×2=154,在化合物X中B的含量为92.2%,则A的相对原子质量为154×(1-92.2%)=12,所以A为碳元素,则n=4,则B的相对分子质量为$\frac{154-12}{4}$=35.5,故B为Cl,X为CCl4,A的氧化物Y为CO2,氧的含量为$\frac{32}{44}$=72.7%,符合题意.
解答 解:A与B(卤素)生成的化合物X表示为ABn,X对氢气的相对密度为77,则ABn的相对分子质量为77×2=154,在化合物X中B的含量为92.2%,则A的相对原子质量为154×(1-92.2%)=12,所以A为碳元素,则n=4,则B的相对分子质量为$\frac{154-12}{4}$=35.5,故B为Cl,X为CCl4,A的氧化物Y为CO2,氧的含量为$\frac{32}{44}$=72.7%,符合题意.
(1)由上述分析可知,X的分子式为CCl4,分子空间构型为正四面体,键角为109°28′,分子中正负电荷重心重合,为非极性分子,
故答案为:CCl4;正四面体;109°28′;非极性;
(2)由上述分析可知,Y的分子式为CO2,分子空间构型为直线形,键角为180°,分子中正负电荷重心重合,为非极性分子,
故答案为:CO2;直线形;180°;非极性.
点评 本题考查较为综合,涉及无机物的推断、物质结构与性质,侧重于学生的基础知识和基本能力的考查,有利于培养学生的科学素养和学习能力,难度不大.


科目:高中化学 来源: 题型:实验题
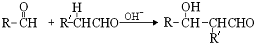
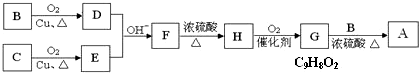
 .
. .
.
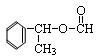 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 Al(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$ Al2O3+3 H2O | B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | ||
| C. | FeO+2 HCl═FeCl2+H2O | D. | FeCl2+2NaOH═Fe (OH)2↓+2NaCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲和乙一定是同分异构体 | B. | 甲和乙的实验式一定相同 | ||
| C. | 甲和乙不可能是同系物 | D. | 甲和乙的分子式一定相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题:
乙醇是一种重要的有机化工原料,它可以用玉米、薯类等为原料经发酵、蒸馏制成.乙醇和汽油经加工处理形成的车用燃料即乙醇汽油.结合有关知识,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z2+能促进水的电离 | |
| B. | 常见单质的熔点:X>Z>Y | |
| C. | 若元素R的某种微粒R2-,则R不一定与Y同主族 | |
| D. | Y与W组成的二元化合物是制耐高温坩埚的常用材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Na | B. | Na2O | C. | Na2O2 | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加大清洁能源的开发利用,提高资源的利用率 | |
| B. | 用CO2合成聚碳酸酯可降解塑料,可以实现“碳”的循环利用 | |
| C. | 加大铅酸蓄电池、含汞锌锰干电池的生产,满足消费需求 | |
| D. | 对工业废水、生活污水净化处理,减少污染物的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| B. | 1molNa与足量O2反应,生成Na2O和Na2O2的混合物,转移2NA个电子 | |
| C. | 标准状况下,2.24L辛烷中所含极性共价键的数目为1.8 NA | |
| D. | 电镀铜时,若阴极得到电子数为2NA个,则阳极质量减少64g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com