
����ʵ�������Ԥ�ڵ�ʵ��Ŀ�Ļ���۾���ȷ����
ѡ�� | ʵ����� | ʵ��Ŀ�Ļ���� |
A | ��FeCl3��Һ��ͨ��Cl2��Ȼ��μ�KSCN��Һ | ��֤Cl2�������Ա�Fe3+ǿ |
B | ��ij��Һ�м��������ữ���Ȼ�����Һ���а�ɫ�������� | ����Һ�в�һ������SO42�� |
C | �ýྻ��Pt˿պȡij��Һ������ɫ��Ӧ������ʻ�ɫ | ����Һ��һ������Na����һ����K�� |
D | ֱ�Ӽ���MgCl2��6H2O���� | ��ȡ��ˮMgCl2���� |

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A���õ��������������Һ�еĵ⻯�أ�5I-+IO-3+3H2O=3I2+6OH-
B����H218O��Ͷ��Na2O2���壺 2H218O + 2Na2O2=4Na++ 4OH��+18O2��
C����100 mL 2 mol/L FeBr2��Һ��ͨ��4��48 L����������£�����ַ�Ӧ��2Fe2++ 2Br��+ 2Cl2 = 2Fe3+ + Br2+4Cl��
D��������Ͷ��ˮ�У�Na��H2O = Na����OH����H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ����Ͽ�и�����ѧ�ڵ�һ�ξ�Ӣ�Կ�����ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͭ��һ������Ũ���ᷴӦ���õ�����ͭ��Һ��NO2��NO�Ļ������2��24L����״��������Щ������һ�����O2����״������Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᡣ������������ͭ��Һ�м���4 mol��L��1NaOH��Һ��Cu2��ǡ����ȫ������������NaOH��Һ�������50 mL,����˵����ȷ���� ( )
A���μӷ�Ӧ��������0��4mol B����������к�NO21��12 L
C���˷�Ӧ������ת�Ƶĵ���Ϊ0��3 mol D���������������Ϊ1��68 L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ӱ�ʡ�����и�һ�ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��12�֣�Ϊ�˳�ȥ�Ȼ�����Ʒ�е�����̼���ƣ�ij��ȤС����������������ʾ��������ʵ�顣

��1������A�Ļ�ѧʽ��________��
��2����������Ȼ�����Һ�����ȥ����A��ʵ�����������___________��
��3��������ʵ������У��ַ������µ����⣺�˷��������������µ����ʡ���������B�ijɷ�Ϊ________(�û�ѧʽ��ʾ)��
��4�����Ǽ���̽������������µķ�������������ܽ⣬�μ����������ٲ�������Ϊֹ��Ȼ�������С��йط�Ӧ�Ļ�ѧ����ʽΪ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������տ������һ�и���10���¿����ۻ�ѧ�Ծ��������棩 ���ͣ������
(13��)��ҵ�ϳ�����ұ��п�����е�п������ZnO��FeO��Fe2O3��CuO��Al2O3�����ʣ�����������ZnSO4��6H2O���壬�乤���������£��й������������ʱ��pH���±���
�������� | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Zn��OH��2 |
��ʼ������pH | 3.3 | 1.5 | 6.5 | 5.4 |
������ȫ��pH | 5.2 | 3.7 | 9.7 | 8.0 |
��1���������������жദ�漰�����ˡ���ʵ�����й��˲�����Ҫʹ�õIJ���������________��
��2���ڡ����Ӣ����У����ټ�������H2O2��Һ��Ŀ����_____��ΪʹFe��OH��3��Al��OH��3������ȫ����Zn��OH��2��������Ӧ������Һ��pH��ΧΪ______��Ϊ��������pH��Χ��ѡ�������Լ���ҩƷ��________��
A��ZnO B����ˮ C������NaOH D��ZnCO3
��3���ڡ����Ӣ����У�����Zn�۵�������_______��������A����������_______��
��4�������£���֪Ksp��Cu��OH��2��=2��10-20��ijCuSO4��Һ��c��Cu2+��=0.02mol/L�����Ҫ����Cu��OH��2��������Ӧ������ҺpH����___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ������ܹ��ɹ�����
A�������������������Ƿ���ʣ�
����
 ��ɫ����
��ɫ���� �������ܽ��˵�������ѱ���
�������ܽ��˵�������ѱ���
B����ȥ�����к��е����������
����



 ����
����
C������ij��Һ���Ƿ���Fe2+
���� ��Һ��ɫ�ޱ仯
��Һ��ɫ�ޱ仯 ��Һ���ɫ����Һ�к���Fe2+
��Һ���ɫ����Һ�к���Fe2+
D��֤����������H2O2�������Ա�I2ǿ��
NaI��Һ
 ��Һ����ɫ�������ԣ�H2O2>I2
��Һ����ɫ�������ԣ�H2O2>I2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������һ�ο������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ����
A��Na2O2����ˮ����O2:Na2O2+H2O= 2Na++2OH-+O2��
B��Fe(OH)3��������Fe(OH)3+3H+ =Fe3++3H2O
C����FeBr2��Һ��ͨ������Cl2��2Fe2����2Br����2Cl2===Br2��2Fe3����4Cl��
D����50 mL 1 mol��L��1������Һ�е�������0.1 mol��L��1Ba(OH)2��Һ��
2Al3����3SO42-��3Ba2����6OH��===2Al(OH)3����3BaSO4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ�����и�����ϰ���ϵ�һ���¿���ѧ�Ծ�A�������棩 ���ͣ�ѡ����
�����й�˵����ȷ����
A��SiO2���������������SiO2����NaOH��Һ��Ӧ
B��SO2����ʹ��ˮ��ɫ������SO2����Ư����
C����ij������Һ����ɫ�ʻ�ɫ�������Һ������һ��ΪNaOH
D��NH3��ˮ��Һ���Ե��磬����NH3�ǵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�������Ĵδ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���0.2 mol/LAl2(SO4��3��Һ�У���μ���1.0 mol/LNaOH��Һ��ʵ������ҺpH��NaOH��Һ����仯��������ͼ������˵����ȷ����
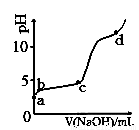
A��a�㣬���ӷ���ʽΪ��Al3+ +3OH- ==Al(OH��3��
B��a��b�Σ���ҺpH���ٽ������������ļ�ʽ����
C��b��c�Σ������OH����Ҫ��������Al(OH��3����
D��d��ʱ��Al(OH��3������ʼ�ܽ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com