
分析 2.38g化合物甲,在空气中充分煅烧后,得固体残留物乙1.82g和标准状况下896mL即0.04mol气体A,该气体能使品红溶液褪色,加热后品红溶液恢复至原色,所以A是SO2,所得固体残留物乙能全部溶于稀硫酸得溶液B,加KSCN溶液,发现溶液变为血红色,所以B是硫酸铁溶液,固体残留物中存在氧化铁,固体残留物部分溶于NaOH溶液中,所以一定含有氧化铝,固体残留物乙1.82g是氧化铝和氧化铁的混合物,其中Fe2O3是0.8g,Al2O3是1.82g-0.8g=1.02g,据此推断化合物甲中一定含有的元素是Fe、Al、S,n(Al)=0.02mol,n(Fe)=0.02mol,n(S)=0.04mol,得到物质的分子式,根据物质的性质进行回答即可.
解答 解:2.38g化合物甲,在空气中充分煅烧后,得固体残留物乙1.82g和标准状况下896mL即0.04mol气体A,该气体能使品红溶液褪色,加热后品红溶液恢复至原色,所以A是SO2,所得固体残留物乙能全部溶于稀硫酸得溶液B,加KSCN溶液,发现溶液变为血红色,所以B是硫酸铁溶液,固体残留物中存在氧化铁,固体残留物部分溶于NaOH溶液中,所以一定含有氧化铝,固体残留物乙1.82g是氧化铝和氧化铁的混合物,其中Fe2O3是0.8g,Al2O3是1.82g-0.8g=1.02g,据此推断化合物甲中一定含有的元素是Fe、Al、S,n(Al)=0.02mol,n(Fe)=0.02mol,n(S)=0.04mol,得到物质的分子式为FeAlS4.
(1)加KSCN溶液,发现溶液变为血红色,所以B中存在铁离子,发生反应为:Fe3++3SCN-=Fe(SCN)3,故答案为:Fe3++3SCN-=Fe(SCN)3;
(2)氧化铝可以和氢氧化钠之间反应生成偏氯酸钠和水,即:Al2O3+2NaOH=2NaAlO2+H2O.故答案为:Al2O3+2NaOH=2NaAlO2+H2O;
(3)气体二氧化硫通入硫酸铁溶液中,发生氧化还原反应,离子反应方程式为:2H2O+2Fe3++SO2=2Fe2++SO42-+4H+,故答案为:2H2O+2Fe3++SO2=2Fe2++SO42-+4H+;
(4)物质甲的分子式为FeAlS4,故答案为:FeAlS4;
(5)金属铁和铝具有还原性,二氧化硫中的S是+4价,具有氧化性,可以发生反应生成低价态的硫化物,故答案为:金属铁和铝具有还原性,二氧化硫中的S是+4价,具有氧化性,可以发生反应生成低价态的硫化物.
点评 本题考查学生物质的分子式的计算,注意物质的性质以及发生反应方程式的书写是关键,学会元素守恒思想的应用是重点,难度中等.


科目:高中化学 来源: 题型:选择题
| 装置 | 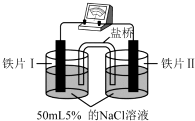 | 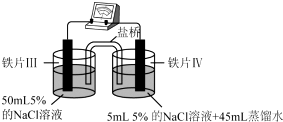 |
| 现象 | 电流计指针未发生偏转 | 电流计指针偏转 |
| A. | “电流计指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀 | |
| B. | 用K3[Fe(CN)6]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极 | |
| C. | 铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,二者的腐蚀速率相等 | |
| D. | 铁片Ⅳ的电极反应式为Fe-3e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某试样焰色反应呈黄色,则试样中含有K+ | |
| B. | 广泛pH试纸测得某碱性溶液的pH为12.5 | |
| C. | 容量瓶不能用作溶解物质的容器 | |
| D. | 粗盐的提纯试验中,滤液在坩埚中加热蒸发结晶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烷烃C5H12的同分异构体中,主链最短的一种系统命名为2,2-甲基丙烷 | |
| B. | 石油分馏和裂化的目的都是为了将长链烃转化为短链烃 | |
| C. | 蛋白质溶液中加入硫酸铜溶液,导致蛋白质变性,失去生理活性 | |
| D. | 高分子化合物(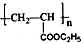 )的单体是CH2=CH2和C2H5COOH )的单体是CH2=CH2和C2H5COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol FeCl3 水解生成的Fe(OH)3胶粒数为lNA | |
| B. | 4.6g有机物C2H6O的分子结构中含有的C一H键数目一定为0.5NA | |
| C. | 标准状况下,11.2 L CO2 与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 1 mol/L AlCl3溶液中含有3NA个Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18 g冰的晶体中含有氢键的数目为2 NA | |
| B. | 11.2 L丙烷(标准状况)中含有σ键的数目为5NA | |
| C. | 2.0 L 0.5 mol/L NaAlO2溶液中含有氧原子的数目为2NA | |
| D. | 1 mol C12与足量NaOH溶液反应,转移电子的数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com