
| A��30 s��X��ƽ����Ӧ����Ϊ0.02 mol?L-1?s-1 | ||
B�����������ݻ�����Ϊԭ��2��������ƽ��ʱZ��Ũ�ȴ���ԭƽ��Ũ�ȵ�
| ||
| C�����¶Ⱥ�������䣬������������2 mol X��1 mol Y����X��Y��ת���ʶ����� | ||
| D���������¶ȣ�X�������������������Ӧ�ġ�H��0 |
| ||
| 30s |
| 1 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
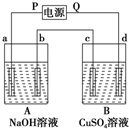 �ö��Ե缫����ͼ��װ�����ʵ�飬����A��B���ձ��ֱ�ʢ��200g 10% NaOH��Һ������CuSO4��Һ��ͨ��һ��ʱ���c������Cu�������ֲ��A����Һ��NaOH����������Ϊ10.23%���Իش�
�ö��Ե缫����ͼ��װ�����ʵ�飬����A��B���ձ��ֱ�ʢ��200g 10% NaOH��Һ������CuSO4��Һ��ͨ��һ��ʱ���c������Cu�������ֲ��A����Һ��NaOH����������Ϊ10.23%���Իش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ʹ���ȱ�����Һ��NH4+��Na+��SO42-��Fe3+ |
| B����ɫ������Һ��K+��HCO3-��SO42-��Al3+ |
| C�����������Ӧ�ܷų���������Һ��NH4+��NO3-��SO42-��Na+ |
| D��ˮ���������c��H+��=1��10-12mol/L����Һ��HCO3-��NH4+��Cl-��Ca2+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
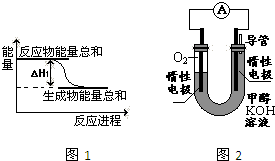 �״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ����ʱ��CaCO3��ˮ�е��ܽ�ƽ��������ͼ��ʾ����֪��25�����ܶȻ�Ϊ2.8��10-9 mol2/L2������˵������ȷ���ǣ�������
����ʱ��CaCO3��ˮ�е��ܽ�ƽ��������ͼ��ʾ����֪��25�����ܶȻ�Ϊ2.8��10-9 mol2/L2������˵������ȷ���ǣ�������| A��x��ֵΪ2��10-5 |
| B��c��ʱ��̼��Ƴ������� |
| C����������ˮ��ʹ��Һ��d��䵽a�� |
| D��b����d���Ӧ���ܶȻ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||
B��
| ||
C��
| ||
D��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CO2������������ |
| B����һ��Ԫ����ɵ�����һ���ǵ��� |
| C������ֻ�����û���Ӧ��ȡ |
| D������Ԫ�صĻ������Ϊ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��H2O2 |
| B��IO3- |
| C��MnO4- |
| D��O3 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com