
| A. | “暖冰”中水分子上的3个原子位于同一条直线上 | |
| B. | 水凝固形成20℃时的“暖冰”所发生的变化是化学变化 | |
| C. | 水是一种非常稳定的化合物,这是由于氢键所致 | |
| D. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
分析 A.根据价层电子对互斥理论判断水分子的空间构型;
B.物理变化和化学变化的本质区别是:是否有新物质生成;
C.化合物的稳定性取决于化学键,与氢键无关;
D.根据题意知,电场作用下,水分子间更易制得“暖冰”.
解答 解:A.水分子中氧原子含有2个σ键和2个孤对电子,所以水分子是V型结构,故A错误;
B.水凝固形成20℃时的“暖冰”没有新物质生成,属于物理变化,故B错误;
C.氢键是分子间作用力的一种,化合物的稳定性取决于分子内化学键的强弱,与氢键无关,故C错误;
D.在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”,否则20℃时,水分子不能瞬间凝固形成冰,故D正确;
故选:D.
点评 本题考查了分子的空间构型、化学变化的判断等知识点,难度不大,注意氢键是分子间作用力的一种,只能影响物质的物理性质,化合物的稳定性源于化学键的强弱,与氢键无关.


科目:高中化学 来源: 题型:解答题
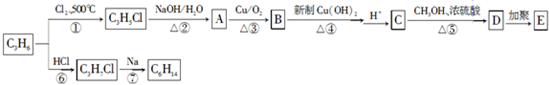
 .
. +6NaBr.
+6NaBr.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

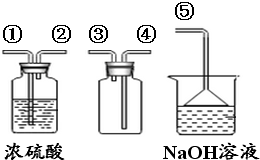
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 容器内A、B、C的浓度之比为1:2:2 | |
| B. | 单位时间消耗0.1 mol•L-1 A,同时消耗0.2 mol•L-1 B | |
| C. | 容器内压强不随时间变化 | |
| D. | 容器内平均相对分子质量不随时间变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两性氧化物 氧化铝 Al2O3 | B. | 盐 小苏打 Na2CO3 | ||
| C. | 碱性氧化物 氧化铁 FeO | D. | 酸性氧化物 碳酸气 CO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和聚氯乙烯都能发生加成反应 | |
| B. | 苯、乙醇和乙酸都可以发生取代反应 | |
| C. | 乙烷、乙醇和乙酸都可以与钠反应生成氢气 | |
| D. | 纤维素和蛋白质水解产物均是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com