
| A. | 第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 工业上金属钠是通过氯碱工业制取的 | |
| C. | ④和⑤步的目的是为了浓缩 | |
| D. | 第③④⑤步中溴元素均被氧化 |
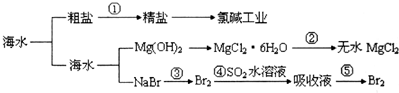
分析 根据转化图可知,①为粗盐提纯,粗盐精制得到精盐溶解制备饱和溶液,通电电解得到氢氧化钠溶液、氯气、氢气,
苦卤中加入石灰乳沉淀镁离子形成氢氧化镁沉淀,过滤得到氢氧化镁沉淀中加入盐酸溶解得到氯化镁溶液,蒸发浓缩,冷却结晶得到氯化镁晶体,②为氯化镁晶体在氯化氢气流中加热得到氯化镁,电解熔融氯化镁得到金属镁;
海水中溴元素以Br-形式存在,工业上用空气吹出法从海水中提取溴,步骤③氯气和溴离子反应生成溴单质;步骤④通过热空气吹出后用二氧化硫吸收得到溴离子,步骤⑤在氯水溶液中重新得到溴单质,据此回答.
A.除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子.盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求;
B.工业用电解熔融的氯化钠冶炼钠;
C.第④步中溴单质被还原为溴离子,第⑤步中溴离子被氧化为溴单质是浓缩富集;
D.根据物质的性质以及变化结合元素化合价的变化判断.
解答 解:A.镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为:加过量的BaCl2溶液,加过量的Na2CO3溶液,加过量的NaOH溶液,过滤,加适量的盐酸;或者,加过量的NaOH溶液,加过量的BaCl2溶液,加过量的Na2CO3溶液,过滤,滤液加适量的盐酸,故A错误;
B.氯碱工业为电解饱和食盐水生成氯气、氢气和氢氧化钠的反应,而工业上用电解熔融的氯化钠冶炼钠,故B错误;
C.第③步将溴离子被氧化为溴单质,第④步中溴单质被还原为溴离子,第⑤步中溴离子被氧化为溴单质,过程的目的是浓缩,故C正确;
D.海水提溴是先通入足量氯气氧化溴离子为溴单质,然后将溴单质还原为溴化氢,再通入适量氯气氧化溴离子为溴单质,④中溴得电子化合价降低,所以溴元素被还原,故D错误;
故选C.
点评 本题考查了海水资源及其综合利用,难点是除杂过程中加入药品的先后顺序,要根据物质的特点来分析解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 将一定量KAl(SO4)2溶液和一定量Ba(OH)2溶液混合,沉淀的质量恰好最大时:Al3++2SO42-+3OH-+2Ba2+═2BaSO4↓+Al(OH)3↓ | |
| B. | 向Ba(OH)2溶液中滴加NaHSO4溶液至混合溶液恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| C. | FeCl3溶液与Cu的反应:Cu+Fe3+═Cu2++Fe2+ | |
| D. | 用Al(OH)3中和过多的胃酸:Al(OH)3+3H+═Al3++3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化镁晶体需在氯化氢气流的氛围中加热失水制得无水氯化镁 | |
| B. | 夏天,打开碳酸饮料会有较多气泡溢出 | |
| C. | 实验室中常用排饱和食盐水的方法收集氯气 | |
| D. | 工业上生产氨气时,采用高温和催化剂等条件 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极的电极反应式为:O2+4H++4e-═2H2O | |
| B. | 溶液中阴离子向正极移动 | |
| C. | 负极的电极反应式为:N2H4+4OH--4e-═4H2O+N2 | |
| D. | 电解质溶液的pH保持不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
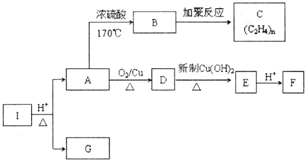 化合物I的分子式为C6H10O4,75%的A溶液常用于医疗消毒,与I相关的反应如图.根据以上信息回答下列问题.
化合物I的分子式为C6H10O4,75%的A溶液常用于医疗消毒,与I相关的反应如图.根据以上信息回答下列问题.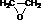 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:3:2 | B. | 5:5:4 | C. | 2:2:3 | D. | 1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
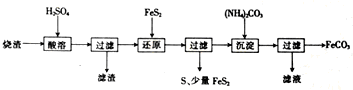
| 离子 | 离子浓度(mol?L-1) | |
| 还原前 | 还原后 | |
| Fe2+ | 0.10 | 2.50 |
| SO42- | 3.50 | 3.70 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com