
4种短周期主族元素W、X、Y、Z的原子序数依次增大,其原子的最外层电子数之和为19,W和X元素原子内质子数之比为1∶2,X2+和Z-的电子数之差为8。下列说法不正确的是 )。
A.W与Y通过离子键形成离子化合物
B.元素原子半径从大到小的顺序是X>Y>Z
C.WZ4分子中W、Z原子通过共价键结合且最外层均达到8电子结构
D.W、Y、Z元素的最高价氧化物对应的水化物中酸性最强的元素是Z
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
由可逆反应测绘出图象如图,纵坐标为生成物在平衡混合物中的百分含量f,下列对该反应的判断正确的是( )
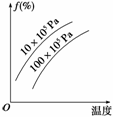
①反应物中一定有气体 ②生成物中一定有气体 ③正反应一定是放热反应 ④正反应一定是吸热反应
A.①③ B.②④ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:95℃时,KW=1.0×10-12.在该温度下,测得0.1mol·L-1Na2A溶液PH=6,则下列说法正确的是

 A.H2A在水溶液中的电离方程式为:H2A H++HA-,HA- H++A2-
A.H2A在水溶液中的电离方程式为:H2A H++HA-,HA- H++A2-
B.(NH4)2A溶液中存在离子浓度关系:c(NH4+)>c(A2-)>c(H+)>c(OH-)
C.0.0lmol·L-l的H2A溶液pH=2
D.等体积等浓度的盐酸与H2A溶液分别与5.6g Zn反应,H2A溶液产生的H2多
查看答案和解析>>
科目:高中化学 来源: 题型:
在容积固定的容器中发生反应:COg)+2H2g)CH3OHg) ΔH<0,各物质的浓度如表所示:
| 浓度 时间 | cCO)/mol·L-1 | cH2)/mol·L-1 | cCH3OH)/mol·L-1 |
| 0 | 0.8 | 1.6 | 0 |
| 2 min | 0.6 | x | 0.2 |
| 4 min | 0.3 | 0.6 | 0.5 |
| 6 min | 0.3 | 0.6 | 0.5 |
下列说法不正确的是 )。
A.2~4 min内用H2表示的平均反应速率为0.3 mol·L-1·min-1
B.达到平衡时,CO的转化率为62.5%
C.反应在第2 min时改变了条件,可能是加入了催化剂
D.反应在第2 min时改变了条件,可能是增加了H2的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 mol红磷转化为1 mol白磷,吸收18.39 kJ热量。
①4Ps,红)+5O2g)===2P2O5s) ΔH1
②4Ps,白)+5O2g)===2P2O5s) ΔH2
则ΔH1与ΔH2的关系正确的是 )。
A.ΔH1=ΔH2 B.ΔH1>ΔH2
C.ΔH1<ΔH2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
图中是部分短周期元素原子半径与原子序数的关系图。则下列说法不正确的是双选) )。
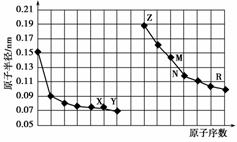
A.Y、R两种元素的气态氢化物及其最高价氧化物的水化物均为强酸
B.简单离子的半径:X>Z>M
C.由X与N两种元素组成的化合物不能与任何酸反应,但能与强碱反应
D.Z单质不能从M与R元素构成的盐溶液中置换出单质M
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是用铁铆钉固定两个铜质零件的示意图,若将该零件置于潮湿空气中,下列说法正确的是( )。
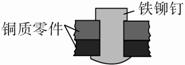
A.发生电化学腐蚀,铜为负极,铜极产生H2
B.铜易被腐蚀,铜极上发生还原反应,吸收O2
C.铁易被腐蚀,铁发生氧化反应:Fe-2e-===Fe2+
D.发生化学腐蚀:Fe+Cu2+===Cu+Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定的溶液中可能大量共存的是( )
A.无色透明溶液中:Al3+、Ca2+、Cl-、HCO3-。
B.含大量Fe3+的溶液中:K+、I-、SO42-、NO3-。
C.与Al反应放出H2的溶液中:NH4+、Na+、NO3-、F- 。
D.由水电离出的c(H+) = 1.0×10-14mol/L的溶液中:Mg2+、K+、Cl-、SO42-。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知常温下在溶液中可发生如下两个离子反应:
Ce4++Fe2+===Fe3++Ce3+
Sn2++2Fe3+===2Fe2++Sn4+
由此可以确定Fe2+、Ce3+、Sn2+三种离子的还原性由强到弱的顺序是( )
A.Sn2+、Fe2+、Ce3+ B.Sn2+、Ce3+、Fe2+
C.Ce3+、Fe2+、Sn2+ D.Fe2+、Sn2+、Ce3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com