
| A. | 化学反应速率是用于衡量化学反应进行快慢的物理量 | |
| B. | 决定化学反应速率的主要因素是反应物本身的性质 | |
| C. | 可逆反应达到化学平衡状态时,反应停止,正、逆反应速率都为零 | |
| D. | 增大反应物浓度或升高反应温度都能加快化学反应速率 |
分析 A、利用化学反应速率来定量表示化学反应进行的快慢;
B、反应物本身的性质是决定化学反应速率的主要因素;
C、化学平衡后,正逆反应速率相等但不等于0;
D、温度越高,反应速率越快,无论该反应是放热反应还是吸热反应.
解答 解:A、化学反应有的快,有的慢,则使用化学反应速率来定量表示化学反应进行的快慢,故A正确;
B、反应物本身的性质是决定反应速率的主要因素,如火药爆炸、食物腐败,故B正确;
C、化学平衡状态时,正逆反应速率相等但不等于0,故C错误;
D、温度越高,反应速率越快,所以锌与稀硫酸反应时,适当提高溶液的温度可加快反应速率,故D正确.
故选C.
点评 本题考查影响化学反应速率的因素,较简单,注意影响反应速率的因素有内因和外因,常见的外因有浓度、温度、压强、催化剂等,但起决定作用的是内因.


 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:解答题
 (1)某同学做如下实验,以检验反应中的能量变化.
(1)某同学做如下实验,以检验反应中的能量变化.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 稀HNO3 | B. | CO | C. | CH3CH2CH2OH | D. | 稀H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正极附近的S042-离子浓度逐渐增大 | |
| B. | 电子通过导线由铜片流向锌片 | |
| C. | 铜片上有H2逸出 | |
| D. | 溶液的pH逐渐变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
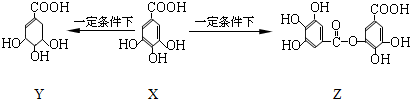
| A. | 1 mol X最多能与2 mol Br2发生取代反应 | |
| B. | Y分子结构中有3个手性碳原子 | |
| C. | Y能发生加成、取代、消去、氧化 | |
| D. | 1 mol Z最多能与7 mol NaOH发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 回答下列问题:
回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓硝酸见光或受热易分解,必须保存在棕色瓶中 | |
| B. | 浓HNO3是种强氧化剂,但只能使湿润蓝色的石蕊试纸显红色而不褪色 | |
| C. | 稀HNO3和活泼金属反应时主要得到氢气 | |
| D. | 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素R位于周期表中第ⅦA族 | |
| B. | RO3-中的R只能被还原 | |
| C. | R2在常温常压下一定是气体 | |
| D. | 若1 mol RO3-参与该反应,则转移的电子的物质的量为10mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com