
下列说法或做法正确的是
A.CO2通入可溶性硅酸盐中析出硅酸沉淀,所以硅酸的酸性大于碳酸
B.一块表面已被氧化为Na2O的钠块10.8g,将其投入100g水中,产生H2 0.2g,则被氧化的钠是4.6g
C.铝比铁活泼,所以铝比铁更容易被腐蚀
D.正常雨水PH等于7,酸雨的PH小于5.6
科目:高中化学 来源:2014-2015山东省聊城市茌平等三县高二上学期期末联考化学试卷(解析版) 题型:选择题
0.4mol CuSO4 和0.4mol NaCl溶于水,配成1L溶液,用惰性电极进行电解,当—个电极得到0.3molCu时,另一个电极上生成的气体在标准状况下的体积是
A.5.6L B.6.72L
C.1.344L D.11.2L
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省菏泽市高一上学期期末考试化学A试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.NaCl溶于水在电流作用下电离成Na+ 和Cl-
B.CaCO3在水中溶解度很小,但溶于水的CaCO3全部电离,所以CaCO3是强电解质
C.某元素在化学反应中由化合态变为游离态(单质),则该元素一定被氧化
D.化合反应一定是氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2014-2015山东省德州市高二2月期末统考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.明矾水解形成的Al(0H)3胶体能杀菌消毒,可用于水的净化
B.镀锡的铁制品比镀锌的铁制品耐用
C.乙醇和乙酸都能溶于水,都是电解质
D.分别与等物质的量的HC1和CH3COOH恰好中和时,消耗NaOH的物质的量相同
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:推断题
(12分)Ⅰ.已知A是一种金属,B溶液能使酚酞试液变红,且焰色反应呈黄色;D、F相遇会产生白烟。A、B、C、D、E、F间有如下变化关系:

(1)B→D反应的化学方程式为 。
(2)F在空气中遇水蒸气产生白雾现象,这白雾实际上是 。
Ⅱ.已知X、Y为有刺激性气味的气体,有以下转化关系,部分产物未标出。
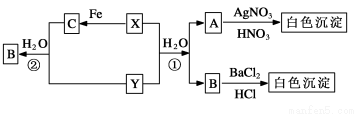
试回答:
(1)写出下列物质的化学式Y________、C________。
(2)反应①的离子方程式为____________,反应②的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:选择题
下列有关实验操作、现象和解释或结论都正确的是
选项 | 实验操作 | 现象 | 解释或结论 |
A | 过量的Fe粉中加入HNO3 ,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀 |
B | CO2通入BaCl2溶液中 | 有白色沉淀出现 | 生成了BaCO3沉淀 |
C | Al箔插入稀 | 无现象 | Al箔表面被 |
D | 用玻璃棒蘸取浓硝酸点到蓝色石蕊试纸上 | 试纸先变红色后褪色 | 浓硝酸有酸性和氧化性 |
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高一上学期期末化学试卷(解析版) 题型:选择题
在25℃、1×105Pa时,等质量的H2、Cl2、CO2、C2H2四种气体中
A.H2分子数最大 B.C2H2原子数最大
C.CO2密度最大 D.Cl2分子间平均距离最大
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省高二上学期期末化学试卷(解析版) 题型:选择题
常温下,0.2 mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
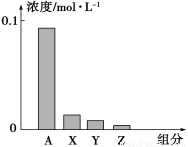
A.HA为强酸
B.图中X表示HA,Y表示OH-,Z表示H+
C.该混合液pH=7
D.该混合溶液中:c(A-)+c(HA)=c (Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省温州市高三一模理综化学试卷(解析版) 题型:推断题
(18分)Ⅰ.A、B、C、D、E、F是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分反应条件略去):
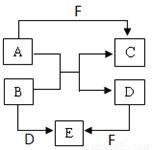
(1)若所有转化都是非氧化还原反应,B、D、E含有同种金属元素,F为强碱(部分产物略去)
则B+D→E的离子方程式为 ,C为同周期元素构成的1∶1型化合物,则C的电子式为 。
(2)若A、D、F为单质,B、C、E为化合物,B为两种非金属元素所组成的化合物,则E的化学式为 ,A+B→C+D的化学方程式为 。
Ⅱ.甲、乙都是二元固体化合物,将32g甲的粉末加入足量浓硝酸并加热,完全溶解得蓝色溶液,向该溶液中加入足量Ba(NO3)2溶液,过滤、洗涤、干燥得沉淀46.6g;滤液中再滴加NaOH溶液,又出现蓝色沉淀。
含乙的矿石自然界中储量较多,称取一定量乙,加入稀盐酸使其全部溶解,溶液分为A、B两等份,向A中加入足量氢氧化钠溶液,过滤、洗涤、灼烧得红棕色固体28g,经分析乙与红棕色固体的组成元素相同,向B中加入8.0g铜粉充分反应后过滤、洗涤、干燥得剩余固体1.6g.
(1)写出构成甲的阴离子的结构示意图 ;32g甲在足量浓硝酸中反应转移的电子数为 ;甲在足量氧气中充分灼烧的化学方程式为 。
(2)乙的化学式 ;稀硫酸溶解乙的化学方程式为 。
(3)将甲在足量氧气中充分灼烧的气体产物通入一定量A溶液中,该反应的离子方程式为 ,设计实验证明此步反应后的溶液中金属元素的化合价 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com