
【题目】图Ⅰ的目的是精炼铜,图Ⅱ的目的是保护钢闸门。下列说法正确的是

A.图Ⅰ中b为纯铜,电解过程中质量减轻,发生的反应为:Cu2++2e-═Cu
B.图Ⅰ中![]() 向a极移动,但不放电
向a极移动,但不放电
C.图Ⅱ中如果a、b间用导线连接时,钢闸门作阴极
D.图Ⅱ中如果a、b间连接直流电源利用外加电流的阴极保护法时,则X必须用锌
 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:
【题目】等体积、等物质的量浓度的硫酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6,则甲、乙两烧杯中的反应情况可能分别是( )
A.甲、乙中都是铝过量
B.甲中铝过量,乙中碱过量
C.甲中酸过量,乙中铝过量
D.甲中酸过量,乙中碱过量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃、101kPa下:
①2Na(s)+ ![]() O2(g)═Na2O(s)△H1=﹣414kJ/mol;
O2(g)═Na2O(s)△H1=﹣414kJ/mol;
②2Na(s)+O2(g)═Na2O2(s)△H2=﹣511kJ/mol.
下列说法正确的是( )
A.①和②生成等物质的量的产物,转移的电子数相同
B.Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
C.25℃、101 kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=+317 kJ/mol
D.①和②产物中的阴阳离子个数比均为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按以下步骤可从![]() 合成
合成![]() (部分试剂和反应条件已略去)
(部分试剂和反应条件已略去)

(1)写出有关物质的结构简式:
A_______________;
C_______________。
(2)指出反应类型:
C→D:___________________________;
F→G:___________________________;
(3)写出下列反应的化学方程式:
D+E→F:_________________________;
F→G:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属腐蚀的电化学原理可用下图模拟。
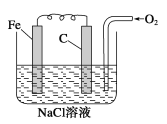
(1)请写出有关电极反应式:_________________________
①铁棒上的电极反应式:_______________________
碳棒上的电极反应式:_________________________
(2)该图所表示的是_________________________(填“析氢”或“吸氧”)腐蚀。
(3)若将O2撤走,并将NaCl溶液改为稀H2SO4溶液,则此图可表示__________(填“析氢”或“吸氧”)腐蚀原理;若用牺牲阳极法来保护铁棒不被腐蚀溶解,即可将碳棒改为_________棒。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的 pH如下表:
实验编号 | c(HA)/molL﹣1 | c(NaOH)/molL﹣1 | 混合溶液pH |
甲 | 0.1 | 0.1 | pH=a |
乙 | 0.2 | 0.2 | pH=9 |
丙 | c1 | 0.2 | pH=7 |
丁 | 0.2 | 0.1 | pH<7 |
下列判断正确的是( )
A.a>9
B.在乙组混合液中由水电离出的c(OH﹣)=10﹣5molL﹣1
C.c1=0.2
D.丁组混合液:c(Na+)>c(A﹣)>c(H+)>c(OH﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
(1)一定温度下,向固定体积为2L的密闭容器中充入SO2和NO2各1mol,发生反应SO2(g)+NO2(g)SO3(g)+NO(g),测得上述反应5min末到达平衡,此时容器中NO与NO2的体积比为3:1,则这段时间内SO2的反应速率υ(SO2)= , 此反应在该温度下的平衡常数K= .
(2)甲醇日趋成为重要的有机燃料,通常利用CO和H2合成甲醇,其反应的化学方程式为CO(g)+2H2(g)CH3OH(g).今在一容积可变的密闭容器中,充有10mol CO和20mol H2用于合成甲醇.CO的平衡转化率(α)与温度(T)、压强(P)的关系如图所示: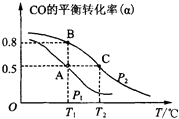
①上述合成甲醇的反应为反应(填“放热”或“吸热”).
②A、B、C三点的平衡常数KA、KB、KC的大小关系为 . A、B两点对应的压强大小关系是PAPB(填“大于”、“小于”或“等于”).
③若将达到平衡状态A时生成的甲醇用于构成甲醇一氧气燃料电池,电解质溶液为KOH浓溶液,则该电池工作时正极的电极反应式为 , 理论上通过外电路的电子最多为 mol.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com