
| A、该反应的还原剂是Cu2S |
| B、当1mol O2发生反应时,还原剂所失去电子的物质的量为4mol |
| C、O2发生了氧化反应 |
| D、CuSO4即是氧化产物,又是还原产物 |


科目:高中化学 来源: 题型:
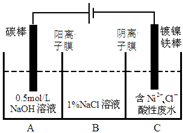 工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是( )已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:
工业上电解法处理含镍酸性废水并得到单质Ni的原理如图所示.下列说法不正确的是( )已知:①Ni2+在弱酸性溶液中发生水解 ②氧化性:| A、碳棒上发生的电极反应:4OH--4e-═O2↑+2H2O |
| B、电解过程中,B中NaCl溶液的物质的量浓度将不断减少 |
| C、为了提高Ni的产率,电解过程中需要控制废水pH |
| D、若将图中阳离子膜去掉,将A、B两室合并,则电解反应总方程式发生改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 操作 | 现象 | 解释或结论 | |||||
| A | 向装有Fe(NO3)2溶液的试管中加入几滴稀H2SO4 | 溶液颜色基本不变 | Fe(NO3)2与H2SO4不反应 | ||||
| B | 向饱和Na2CO3溶液中通入足量CO2 | 溶液变浑浊 | 析出了NaHCO3晶体 | ||||
| C | 将Al2(SO4)3溶液蒸干 | 有白色固体生成 | Al3++3H2O
| ||||
| D | 将Na放入CuSO4溶液中 | 有红色固体析出 | 2Na+Cu2+═Cu+2Na+ |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18g的D216O中含有的中子数为9NA |
| B、物质的量浓度均为1.0mol/L的硫酸与高氯酸(HClO4)溶液中含有的氧原子数均为4NA |
| C、33.6L NO2溶于足量的水得到的溶液中含有的NO3-数为NA |
| D、32g铜发生氧化还原反应,一定失去NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、与Al反应放出H2的溶液:Mg2+、Ca2+、HCO3-、NO3- | ||
| B、10mol?L-1的浓氨水:Al3+、NH4+、NO3-、I- | ||
| C、0.1 mol?L-1KMnO4溶液:Na+、Fe2+、SO42-、Cl- | ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、a组:制备少量乙酸乙酯 |
| B、b组:除去粗盐水中的泥沙 |
| C、c组:用CCl4提取碘水中的碘 |
| D、d组:配制100 mL 1.00 mol/L NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 近年来,碳和碳的化合物在生产生活实际中应用广泛.
近年来,碳和碳的化合物在生产生活实际中应用广泛.| t(℃) | 750 | 850 | 1000 |
| CO% | 0.7 | 2/3 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com