
CuI是一种不溶于水的白色固体,它可由反应2Cu2++4I-=2CuI+I2而得到。现以石墨为
阴极,以Cu为阳极电解KI溶液,通电前向电解液中加入少量酚酞和淀粉溶液。电解
开始不久阴极区溶液呈红色,而阳极区溶液呈蓝色,对这些现象的正确解释是( )
①阴极2H++2e-= H2↑,使c(OH-)>c(H+) ②阳极4OH--4e-=2H2O+O2↑,O2将I-氧化为I2,I2遇淀粉变蓝 ③阳极2I--2e-=I2,I2遇淀粉变蓝 ④阳极2Cu-4e-+4I-=2CuI+I2,I2遇淀粉变蓝
A.①② B.①③ C.①④ D.③④
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:
露置于空气中一段时间后的水玻璃会浑浊。向此浑浊溶液中加入稀盐酸,会生成白色胶状沉淀,同时伴随有气泡产生。用化学方程式解释产生上述现象的原因:
(1)溶液变浑浊:____________________,说明硅酸的酸性比碳酸_______。(填“强”或“弱”)
(2)生成白色胶状沉淀:__________________;
(3)产生气泡:____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
自来水常用Cl2消毒,某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是
A.AgNO3 B.FeCl2 C.Na2SO3 D.AlCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
本题列举的四个选项是4位同学在学习“化学反应速率和化学平衡”一章后,联系工业
生产实际所发表的观点,你认为不正确的是( )
A.化学反应速率理论是研究怎样在一定时间内快出产品
B.化学平衡理论是研究怎样使用有限原料多出产品
C.化学反应速率理论是研究怎样提高原料转化率
D.化学平衡理论是研究怎样使原料尽可能多地转化为产品
查看答案和解析>>
科目:高中化学 来源: 题型:
常温时,向pH=12的Ba(OH)2溶液中加入等体积的下列溶液后,滴入酚酞试液出现红
色,该溶液应该是( )
A.pH=2的硫酸溶液 B.pH=2的醋酸溶液
C.0.05mol/L盐酸溶液 D.0.05mol/LNa2SO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
类比法是化学学习过程中一种重要方法,以下类比关系正确的是
A.工业上可以电解熔融的氯化镁或氯化铝制得相应的金属单质
B.醇和酚中都有羟基,都可以和氢氧化钠溶液反应
C.二氧化碳和二氧化硫都是氧化物,两者都不能和氯化钙溶液反应
D.氧化铁和氧化亚铁都是碱性氧化物,和硝酸反应都只生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、D、E、G六种短周期元素的原子序数依次递增。X、Y、D元素的基态原子中电子层数与未成对电子数均相等;D、E属于同族元素,G的单质和ED2化合物均具有漂白性;R元素的M层全满,N层只有1个电子。
请回答下列问题:(用对应的元素符号表示)
(1)R元素在元素周期表分区中属于______区元素,Y、Z、D三种元素中电负性由小到大的顺序是_________。
(2)X3D+的中心原子杂化轨道类型是__________,该离子的立体构型是 。
(3)向RED4的水溶液中加入ZX3的水溶液至过量,有关反应的离子方程式是 。
(4)向RG2的水溶液通入ED2,产生白色沉淀RG,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某兴趣小组探究以芒硝Na2SO4·10H2O和CaO为原料制备Na2CO3。
29.将CaO水化后,与芒硝形成Na2SO4-Ca(OH)2-H2O三元体系,反应后过滤,向滤液中通入CO2,期望得到Na2CO3。三元体系中反应的离子方程式为:
SO42-+ Ca(OH)2(s)+2H2O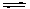 CaSO4·2H2O(s)+2 OH-
CaSO4·2H2O(s)+2 OH-
该反应的平衡常数表达式K=_________________________。
往Na2SO4-Ca(OH)2-H2O三元体系中添加适量的某种酸性物质,控制pH=12.3 [即c(OH-)=0.02mol/L],可使反应在常温下容易进行。反应后过滤,再向滤液中通入CO2,进一步处理得到Na2CO3。
30.在Na2SO4-Ca(OH)2-H2O三元体系中不直接通入CO2,其理由是_________________
______________________________________________。
31.添加的酸性物质须满足的条件(写出两点)是_____________、______________。
32.用平衡移动原理解释添加酸性物质的理由:____________________________________;
以HA表示所添加的物质,则总反应的离子方程式可写为_______________________。
33.Na2CO3溶液中存在水解平衡:CO32-+H2O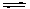 HCO3-+OH-。下列说法错误的是_________。
HCO3-+OH-。下列说法错误的是_________。
a.加水稀释,溶液中所有离子的浓度都减小 b.通入CO2,溶液pH减小
c.加入NaOH固体,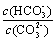 减小 d.稀释溶液,平衡常数增大
减小 d.稀释溶液,平衡常数增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com