
【题目】(1)含氢原子为0.2×6.02×1024个的NH4HCO3,其质量是___,其中含氧原子的物质的量为___。3.6克水中含有质子数为___(阿伏伽德罗常数为NA)。
(2)现实验室要用12mol·L-1氢氧化钠溶液来配制浓度为0.6mol·L-1的稀氢氧化钠溶液100mL,则需要这种浓碱的体积是___mL。需要用托盘天平称量___克氢氧化钠才能配制成0.5mol·L-1的氢氧化钠溶液100mL。
(3)将标况下aLHCl气体溶于配制成1L盐酸溶液,所得溶液密度为dg/cm3,则所得溶液物质的量浓度为___mol/L,该溶液中溶质的质量分数为___。
(4)在标准状况下,某气体A的密度是1.25g·L-1,则它的摩尔质量是___,同温同压下该气体相对于氢气的密度是___;在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,此混合气体的平均相对分子质量是___,混合物中CO和CO2物质的量之比是___。
【答案】31.6克 1.2mol 2NA 5.0 2.0 ![]()
![]() 28g/mol 14 40 1:3
28g/mol 14 40 1:3
【解析】
(1)含氢原子为0.2×6.02×1024个,则氢原子的物质的量为![]() ,则NH4HCO3的物质的量=2mol×
,则NH4HCO3的物质的量=2mol×![]() =0.4mol,其质量=0.4mol ×79g/mol=31.6g;其中含氧原子的物质的量=0.4mol×3=1.2mol;3.6克水的物质的量=
=0.4mol,其质量=0.4mol ×79g/mol=31.6g;其中含氧原子的物质的量=0.4mol×3=1.2mol;3.6克水的物质的量=![]() =0.2mol,一个水分子中含有10个质子,则0.2mol水中含有质子数为0.2mol×10×NA=2NA,
=0.2mol,一个水分子中含有10个质子,则0.2mol水中含有质子数为0.2mol×10×NA=2NA,
答案为:31.6克;1.2mol;2NA;
(2)由浓溶液配制稀溶液,溶质的物质的量不变,可用稀释公式解题,设需要12mol·L-1氢氧化钠溶液的体积为V,则12mol·L-1V=0.6mol·L-1×100mL,则V=5.0ml;配制成0.5mol·L-1的氢氧化钠溶液100mL,溶质氢氧化钠的物质的量=0.5mol·L-1×0.1L=0.05mol,其质量为0.05mol×40g/mol=2.0g,
答案为:5.0;2.0;
(3)将标况下aLHCl气体的物质的量=![]() =
=![]() ,盐酸溶液的体积为1L,则所得溶液物质的量浓度为
,盐酸溶液的体积为1L,则所得溶液物质的量浓度为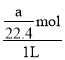 =
=![]() mol/L;根据c=
mol/L;根据c=![]() ,该溶液中溶质的质量分数
,该溶液中溶质的质量分数![]() =
= =
=![]() ,
,
答案为:![]() ;
;![]() ;
;
(4)在标准状况下,1molA的体积为22.4L,则1molA的质量=![]() ,则摩尔质量是28g/mol;同温同压下,气体的密度之比等于摩尔质量之比,该气体相对于氢气的密度是
,则摩尔质量是28g/mol;同温同压下,气体的密度之比等于摩尔质量之比,该气体相对于氢气的密度是![]() =14;在标准状况下,由CO和CO2组成的混合气体为6.72L,混合气体的物质的量=
=14;在标准状况下,由CO和CO2组成的混合气体为6.72L,混合气体的物质的量=![]() =0.3mol,质量为12g,此混合气体的平均相对分子质量=
=0.3mol,质量为12g,此混合气体的平均相对分子质量=![]() =40g/mol,根据十字交叉法:
=40g/mol,根据十字交叉法:
 ,则
,则![]() ,
,
答案为:28g/mol;14;40;1:3。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】测定有机化合物中碳和氢的组成常用燃烧分析法,下图是德国化学家李比希测定有机物组成的装置,氧化铜作催化剂,在750℃左右使有机物在氧气流中全部氧化为CO2和H2O,用含有固体氢氧化钠和氯化钙的吸收管分别吸收CO2和H2O。

试回答下列问题:
(1)甲装置中盛放的是________,甲、乙中的吸收剂能否颠倒?________。
(2)实验开始时,要先通入氧气一会儿,然后再加热,为什么? _____________________。
(3)将4.6 g有机物A进行实验,测得生成5.4 g H2O和8.8 g CO2,则该物质中各元素的原子个数比是________。
(4)经测定,有机物A的核磁共振氢谱图显示有三组峰,则A的结构简式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。
(1)某同学用含钠元素的不同类别物质制备NaCl。请再列举3种反应:
①2Na+Cl2![]() 2NaCl
2NaCl
②___;
③___;
④___。
(2)粗盐中一般含有CaCl2、MgCl2、CaSO4和MgSO4杂质。从粗盐制得精盐的过程如下:

①写出MgCl2、CaSO4的电离方程式:___、___。
②各操作分别是:操作a___、操作b___、操作c___。
③试剂Ⅰ是___。
④加入试剂Ⅱ所发生的离子方程式为___,加入试剂Ⅲ所发生的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下四种溶液,有关叙述不正确的是
序号 | ① | ② | ③ | ④ |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A. ③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B. ②③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C. 分别加水稀释10倍,四种溶液的pH①>②>④>③
D. V1L④与V2L①溶液混合后,若混合后溶液pH=7,则V1<V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制500mL0.1mol/LNa2CO3,溶液回答下列问题
(1)配制Na2CO3溶液时需用的主要仪器有托盘天平、滤纸、烧杯、药匙、量筒、___、___、___。
(2)配制溶液过程如下:
A.用托盘天平称取Na2CO3·10H2O晶体___g;
B.将固体置于烧杯中,用量筒向其中加水溶解,并恢复至室温;
C.用玻璃棒引流,将溶液转移至容量瓶;
D.洗涤玻璃棒和烧杯2-3次,将洗涤液都转移入容量瓶中;
E.___;
F.继续向容量瓶中注水,至液面离容量瓶颈刻度线下___cm时,改用___滴加蒸馏水至液面与刻度线相切;
G.盖好瓶塞,用食指抵住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次摇匀;
H.将溶液转移至试剂瓶中,贴上标签,标注试剂名称、浓度及配制时间。
(3)若实验遇下列情况,溶液的浓度是偏高,偏低还是不变?
A.加水时超过刻度线___;
B.溶解后未冷却到室温就转入容量瓶___;
C.容量瓶内壁附有水珠而未干燥处理___;
D.定容时仰视___;
E.上下颠倒摇匀后液面低于刻度线___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合液中逐滴加入稀盐酸,生成气体的量随稀盐酸加入量的变化关系如下图所示。则下列离子组在对应的溶液中一定能大量共存的是( )
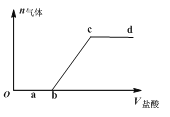
A.a点对应溶液中:Ca2+、Mg2+、Br-、NO3—
B.b点对应溶液中:Al3+、Fe3+、MnO4—、NO3—
C.c点对应溶液中:Na+、Ca2+、NO3—、Cl-
D.d点对应溶液中:F-、NO3—、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是
A.n(Cl2)∶n(Fe)=5∶4;5Cl2+4Fe![]() 2FeCl2+2FeCl3
2FeCl2+2FeCl3
B.n(Cl2)∶n(FeBr2)=1∶1;Fe2++2Br+Cl2=Fe3++Br2+2Cl
C.n(MnO4-)∶n(H2O2)=2∶3;2MnO4-+3H2O2+6H+=2Mn2++4O2↑+6H2O
D.n(Fe) ∶n[HNO3(稀)]=1∶3;4Fe+12H++3NO3-=3Fe2++Fe3++3NO↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制Cl2的反应为4HCl(浓)+MnO2![]() MnCl2+Cl2↑+2H2O.下列说法错误的是( )
MnCl2+Cl2↑+2H2O.下列说法错误的是( )
A. 还原剂是HCl,氧化剂是MnO2
B. 每生成1 molCl2,转移电子的物质的量为2 mol
C. 每消耗1 molMnO2,起还原剂作用的HCl消耗4mol
D. 生成的Cl2中,除含有一些水蒸气外,还含有HCl杂质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绚丽多彩的无机颜料的应用曾创造了古代绘画和彩陶的辉煌。硫化镉(CdS)是一种难溶于水的黄色颜料,其在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是

A. 图中a和b分别为T1、T2温度下CdS在水中的溶解度
B. 图中各点对应的Ksp的关系为:Ksp(m)=Ksp(n)<Ksp(p)<Ksp(q)
C. 向m点的溶液中加入少量Na2S固体,溶液组成由m沿mpn线向p方向移动
D. 温度降低时,q点的饱和溶液的组成由q沿qp线向p方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com