
| ���� | ������ƽ�������룩 | С�ձ� | ����ǯ | ������ | ҩ�� | ��Ͳ |
| ���� |  |  |  |  |  |  |
| ��� | a | b | c | d | e |
| ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶� t2/��[ | �¶Ȳ�ƽ��ֵ ��t2-t1��/�� | ||
| H2SO4 | NaOH | ƽ��ֵ | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
���� ��1�����ݹ�ʽm=nM=cVM�������������Ƶ�����������û��245mL������ƿ��
��2����������Ҫ�ڲ��������г��������ݳ������������������õ��������ش�
��1����������кͷ�Ӧ����1molҺ̬ˮʱ�ų�57.3kJ��������д�Ȼ�ѧ����ʽ��
��2�������ж��¶Ȳ����Ч�ԣ�Ȼ������¶Ȳ�ƽ��ֵ��
���ȸ���Q=m•c•��T���㷴Ӧ�ų���������Ȼ����ݡ�H=-$\frac{Q}{n}$kJ/mol�������Ӧ�ȣ�
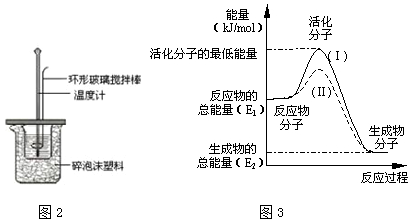
��3��������ͼ�������Ӧ��������������������������Ӧ���ȣ���Ӧ���ʱ�=�����������-��Ӧ���������
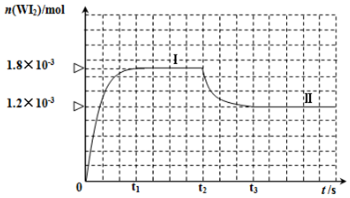
�ڶ���ͬһ��Ӧ��ͼ�����ߣ� II����ʵ�ߣ� I����ȣ���ܴ�ͣ�����ӵİٷ������࣬��Ӧ���ʼӿ죬˵����Ӧ�Ļ�ܽ����ʱ䲻�䣬ƽ�ⲻ�������Ӱ���������ʵ�Ԫ�ط����жϣ�
��� �⣺��1��û��245mL������ƿ��������250mL������ƿ����Ҫ����NaOH����m=nM=cVM=0.5mol/L��0.25L��40g/mol=5.0g��
�ʴ�Ϊ��5.0��
��2����������Ҫ��С�ձ��г������������������������õ���������ƽ���ձ���ҩ�ף�
�ʴ�Ϊ��abe��
��1����֪ϡǿ�ᡢϡǿ�Ӧ����1molҺ̬ˮʱ�ų�57.3kJ��������ϡ���������������ϡ��Һ����ǿ���ǿ���ϡ��Һ����Ӧ���Ȼ�ѧ����ʽΪ��
$\frac{1}{2}$H2SO4��aq��+NaOH��aq��=$\frac{1}{2}$Na2SO4��aq��+H2O��l����H=-57.3kJ/mol��
�ʴ�Ϊ��$\frac{1}{2}$H2SO4��aq��+NaOH��aq��=$\frac{1}{2}$Na2SO4��aq��+H2O��l����H=-57.3kJ/mol��
��2����4���¶Ȳ�ֱ�Ϊ��4.0�棬4.1�棬3.9�棬4.1�棬4�����ݶ���Ч���¶Ȳ�ƽ��ֵ=$\frac{4.0��+4.1��+3.9��+4.1��}{4}$=4.0�棻
�ʴ�Ϊ��4.0��
��50mL0.50mol/L����������30mL0.50mol/L������Һ�����кͷ�Ӧ����ˮ�����ʵ���Ϊ0.05L��0.50mol/L=0.025mol����Һ������Ϊ��80ml��1g/ml=80g���¶ȱ仯��ֵΪ��T=4�棬������0.025molˮ�ų�������ΪQ=m•c•��T=80g��4.18J/��g•�棩��4.0��=1337.6J����1.3376KJ������ʵ���õ��к��ȡ�H=-$\frac{1.3376kJ}{0.025mol}$=-53.5 kJ/mol��
�ʴ�Ϊ��-53.5kJ/mol��
��3��������ͼ�������Ӧ��������������������������Ӧ���ȣ���Ӧ���ʱ��H=�����������-��Ӧ�������=��E2-E1��kJ/mol��
�ʴ�Ϊ�����ȣ���E2-E1��kJ/mol��
�ڶ���ͬһ��Ӧ��ͼ�����ߣ� II����ʵ�ߣ� I����ȣ���ܴ�ͣ�����ӵİٷ������࣬��Ӧ���ʼӿ죬˵����Ӧ�Ļ�ܽ����ʱ䲻�䣬ƽ�ⲻ������ѧ��Ӧ����Ӱ�������У������д����ã��������п���ʹ���˴�����
�ʴ�Ϊ��ʹ���˴�����
���� ������Ҫ�����ȷ�Ӧ�ȵIJⶨ����㣬��ѧ��Ӧ�������仯�뷴Ӧ���ʱ��ϵ����Ŀ�ѶȲ���ע���ʱ�ͻ�ܼ��㷽�����к��ȵĸ����Լ��ⶨ��Ӧ�ȵ��������⣮


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol�����к��е�ԭ����ĿΪNA | |
| B�� | 5.85g NaCl�к��е�����������ĿΪ1.6NA | |
| C�� | 2mol NO��1mol O2��ϣ���ַ�Ӧ��ת�Ƶĵ�����ĿΪ4NA | |
| D�� | 25��ʱ��1L 0.1mol•L-1 Na2S��Һ�е���������ĿС��0.1NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��3��6 | B�� | 2��3��9 | C�� | 9��3��1 | D�� | 1��2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ���� | C�� | ���� | D�� | ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
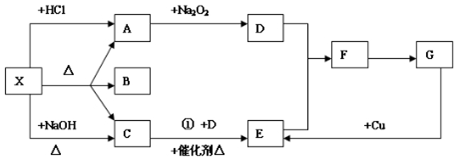
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��2��4-���ױ� 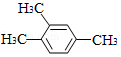 | B�� | 3-��-1-��ϩ | C�� | 2-��-1-���� 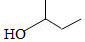 | D�� | 1��3-�������  |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com