
【题目】下列说法正确的是
A. 石墨和C60互为同位素
B. CH4和CH3CH3互为同系物
C. 14CO2的摩尔质量为46
D. 3517Cl、3717Cl 为不同的核素,有不同的化学性质
科目:高中化学 来源: 题型:
【题目】已知阿伏伽德罗常数可表示为NA,则下列说法正确的是
A. 任何气体单质在标准状况下体积约为22.4L,则一定含有2NA个原子
B. 常温常压下,22g氧气和26g臭氧所含氧原子总数为3NA
C. 常温常压下,22.4LH2O中含有的氢原子数为2NA
D. 标准状况下,0.3molCO2中含有氧原子数0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了将混有K2SO4、MgSO4的KNO3固体提纯,并制得纯净的KNO3溶液E,某学生设计如下实验方案:
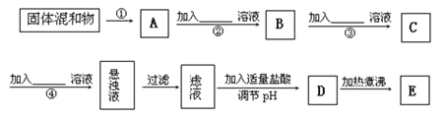
(1)操作①主要是将固体溶解,则所用的主要玻璃仪器是_____ __、____ ___。
(2)操作②~④加入的试剂依次可以为(写化学式):______________________________;
(3)如何判断SO42-已除尽?_________ ____ ___;
(4)写出加入适量盐酸调PH反应的离子方程式_____________________ ____;
(5)该同学的实验设计方案是否严密?请说明理由:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)NaHCO3溶液中存在多种平衡关系,写出相应平衡关系所对应的离子方程式:_ _ 。
NaHCO3溶液显碱性的原因: _ 。
NaHSO4溶液显酸性的原因: 。
(2)在101kPa时,H2在1.00molO2中完全燃烧生成2.00mol液态H2O。放出571.6kJ的热量,表示H2燃烧热的热化学方程式为____________ 。
(3)1.00L 1.00mol/L H2SO4溶液与2.00L 1.00mol/L NaOH溶液完全反应,放出114.6kJ的热量,表示其中和热的热化学方程式为______________ _ 。
(4)已知C(s)+O2(g)=CO2(g) △H1=-393.5kJ/mol,
2CO(g)+O2(g)=2CO2(g) △H2=-566.0kJ/mol,
C(s)+0.5O2(g)=CO(g) △H3=akJ/mol,则a=__________
(5)已知N2(g) +3H2(g) ![]() 2NH3(g)的平衡常数为K1,0.5 N2(g)+1.5H2(g)
2NH3(g)的平衡常数为K1,0.5 N2(g)+1.5H2(g) ![]() NH3(g) 的平衡常数为K2,NH3(g)
NH3(g) 的平衡常数为K2,NH3(g) ![]() 0.5 N2(g)+1.5H2(g) 的平衡常数为K3,写出K1和K2的关系式__________,写出K2和K3的关系式____________,写出K1和K3的关系式_____________
0.5 N2(g)+1.5H2(g) 的平衡常数为K3,写出K1和K2的关系式__________,写出K2和K3的关系式____________,写出K1和K3的关系式_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上常用铁质容器盛装冷浓硫酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动。
【探究一】
(1)甲同学将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________________。
【探究二】
(2)另称取铁钉6.0 g放入15.0 mL浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。乙同学取336 mL(标准状况)气体Y通入足量溴水中,发生反应:SO2+Br2+2H2O===2HBr+H2SO4然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33 g。由此推知气体Y中SO2的体积分数为________。
分析上述实验中SO2体积分数的结果,丙同学认为气体Y中还可能含有H2和Q气体。为此设计了下列探究实验装置(图中夹持仪器省略):
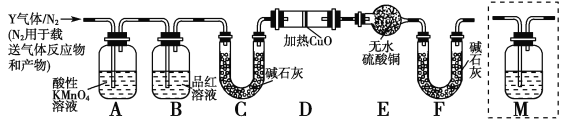
(3)装置B中试剂的作用是________。
(4)认为气体Y中还含有Q的理由是_____________________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于________(选填序号)。
a.A之前 b.A—B间 c.B—C间 d.C—D间
(6)如果气体Y中含有H2,预计实验现象应是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某地今年启动11项工程治理氮磷污染,以保护空气环境和饮用水源。下面是有关氮污染防治及处理方法。据此回答下列问题:
(1)已知CO可将NO转化为N2,某研究小组在实验室研究反应条件对NO转化率的影响。
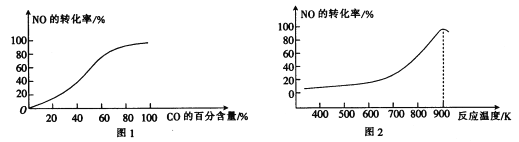
①由图1可知CO的百分含量越高,NO的转化率越______________(填“高”或“低”)。
②当![]() 时,NO的转化率随温度的变化如图2所示,则应控制反应的最佳温度在___________左右。
时,NO的转化率随温度的变化如图2所示,则应控制反应的最佳温度在___________左右。
(2)在催化剂存在的条件下,用H2将NO还原为N2。已知:
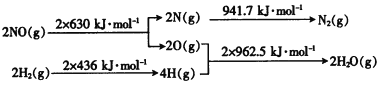
则氢气和一氧化氮反应生成氮气和水蒸气的热化学方程式是___________________。
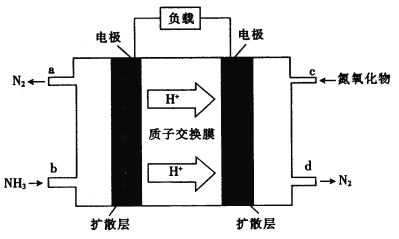
(3)氨气一氮氧化物燃料电池可用于处理氮氧化物,防止空气污染,其装置如图所示。通入氨气的电极为_____________(填“正极”或“负极”)。负极的电极反应式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C2H6O 的可能是甲醚或乙醇,可采用化学方法及物理方法加以鉴别,下列鉴别方法中不能对二者进行鉴别的是
A. 利用金属钠或者金属钾 B. 利用燃烧法
C. 利用红外光谱法 D. 利用核磁共振氢谱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种短周期元素,A、B同主族,C、D同周期,B、E同周期。气体A2与气体C2混合后点燃能够发生爆炸,且产物在常温常压下是一种无色无味的液体。B、C、E简单离子的核外电子排布相同。E的最高价氧化物可与B的最高价氧化物的水化物反应生成一种易溶于水的的盐,D能形成自然界硬度最大的单质。请根据上述所提供的信息回答下列问题。
(1)写出A、B两种元素的元素名称:A________、B________写出D的最高价氧化物的电子式 。
(2)写出由B和C两元素形成的原子个数比为1:1的化合物F的电子式 ,其存在的化学键是
(3)写出F和A2C反应的离子方程式:____________________。
(4)用电子式表示B2C形成的过程:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.甲苯分子中共平面的原子最多是12个
B.对二甲苯分子中有4个碳原子在一条直线上
C.1—丁烯分子中的4个碳原子一定不在同一平面内
D.2—丁烯分子中的4个碳原子一定不在同一平面内
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com