
| A. | 熔沸点较高 | B. | 能溶解于水 | C. | 溶液能导电 | D. | 受热易分解 |
科目:高中化学 来源: 题型:多选题
| A. | 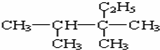 ,3,3-三甲基戊烷 ,3,3-三甲基戊烷 | B. | 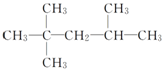 2,2,4三甲基戊烷 2,2,4三甲基戊烷 | ||
| C. | (CH3CH2)2CHCH3 3甲基戊烷 | D. | 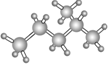 异戊烷 异戊烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol•L-1H2S水溶液中,H2S、HS-和S2-粒子数目之和为0.01NA | |
| B. | 0.16g氨基中含有N-H键的数目为0.02NA | |
| C. | 0.1mol CaO与0.2mol水完全反应后,溶液中Ca2+的数目为0.1NA | |
| D. | 2.24L氯气通入足量的NaOH溶液中,转移的电子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2和SiO2 | B. | CCl4和KCl | C. | NaOH和CaCl2 | D. | CO2和H2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
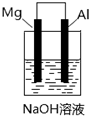
| A. | 该装置中镁条作负极 | |
| B. | 该装置中镁条上无气泡产生 | |
| C. | 该装置中电子从铝条经导线流向镁条 | |
| D. | 该装置中铝条表面产生气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0g H218O与T2O的混合物中所含中子数 | |
| B. | 250mL 1mol/LFeCl3溶液中,阴、阳离子总数 | |
| C. | 标准状况下,7g某单烯烃A中的C-H键数 | |
| D. | 200mL 10mol/L盐酸与足量MnO2反应,转移电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
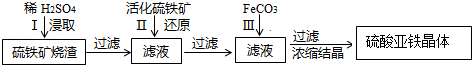
| pH | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 5.8 | 8.8 |
| Fe(OH)3 | 1.1 | 3.2 |
| Al(OH)3 | 3.0 | 5.0 |
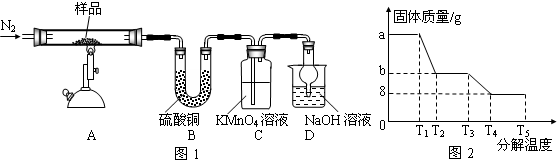
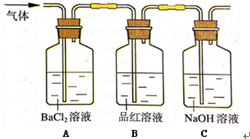 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比2:1反应 | |
| B. | Ba(OH)2与NaHSO4两溶液的溶质按物质的量之比1:2反应 | |
| C. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比2:1反应 | |
| D. | Ba(OH)2与NH4HSO4两溶液的溶质按物质的量之比1:2反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com