


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
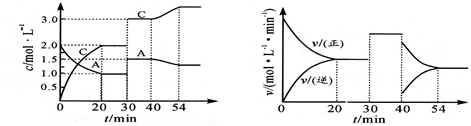
| c2(C) |
| c(A)×c(B) |
| c2(C) |
| c(A)×c(B) |
| 容器 | 甲 | 乙 | 丙 |
| 起始投料 | 1molA和1molB | 2molC | 2molA和2molB |
| A的平衡浓度 | C1 | C2 | C3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2012届安徽省高二下学期期中考试化学试卷(理科) 题型:选择题
一定温度下,某密闭容器里发生如下反应:CO(g) + H2O(g) CO2(g) + H2(g)(正反应为吸热反应),当反应达到平衡时,测量容器中各物质的物质的量均为n mol,欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是
CO2(g) + H2(g)(正反应为吸热反应),当反应达到平衡时,测量容器中各物质的物质的量均为n mol,欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是
①升高温度 ②增大压强 ③再通入n mol CO2和n mol H2 ④恒容再加入2n mol CO和2n mol H2O(g)
A.①② B.②④ C.③④ D.①②③
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com