
下列实验装置设计正确且能达到目的的是
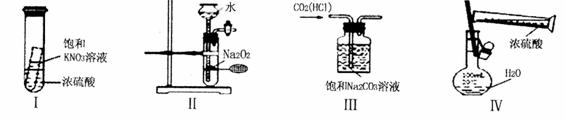
A.实验I:静置一段时间,小试管内有晶体析出 B. 实验II:制取氧气
C. 实验III除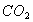 气体中的HCL D.实验IV:配制一定物质的量浓度的稀硫酸
气体中的HCL D.实验IV:配制一定物质的量浓度的稀硫酸
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
分析如图所示的四个原电池装置,结论正确的是( )
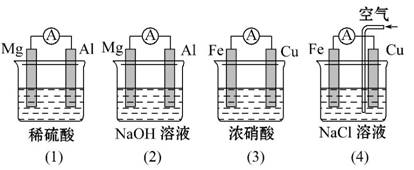
A.(1)(2)中Mg作负极,(3)(4)中Fe作负极
B.(2)中Mg作正极,电极反应式为6H2O+6e-====6OH-+3H2↑
C.(3)中Fe作负极,电极反应式为Fe-2e-====Fe2+
D.(4)中Cu作正极,电极反应式为2H++2e-====H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
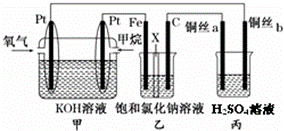
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为阳离子交换膜. 请按要求回答相关问题:
(1)甲烷燃料电池正极反应式为 .
(2)石墨电极(C)的电极反应式为 .
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁电极上生成的气体体积为 L.
(4)丙中两根铜丝电极的质量均为64g,电解质为500mL 0.1mol•L﹣1H2SO4溶液.电解一段时间后,a端收集到1.12L气体(标准状况下),取出电极,对电极进行干燥并称重,测得b电极的质量减少6.4g.求此时所得溶液的物质的量浓度.
查看答案和解析>>
科目:高中化学 来源: 题型:
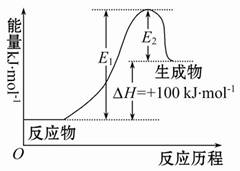
某反应的ΔH=+100 kJ·mol-1,下列有关该反应的叙述正确的是( )
A.正反应活化能小于100 kJ·mol-1
B.逆反应活化能一定小于100 kJ·mol-1
C.正反应活化能不小于100 kJ·mol-1
D.正反应活化能比逆反应活化能大100 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度时,在2 L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
(1)根据表中数据,在图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
| t/min | X/mol | Y/mol | Z/mol |
| 0 | 1.00 | 1.00 | 0.00 |
| 1 | 0.90 | 0.80 | 0.20 |
| 3 | 0.75 | 0.50 | 0.50 |
| 5 | 0.65 | 0.30 | 0.70 |
| 9 | 0.55 | 0.10 | 0.90 |
| 10 | 0.55 | 0.10 | 0.90 |
| 14 | 0.55 | 0.10 | 0.90 |

(2)体系中发生反应的化学方程式是_____________________________________
___________________________________________________________________;
(3)列式计算该反应在0~3 min时间内产物Z的平均反应速率:____________
_____________________________________;
(4)该反应达到平衡时反应物X的转化率α等于______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是:
A. 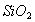 是酸性氧化物,能与溶液反应
是酸性氧化物,能与溶液反应
B. 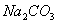 和
和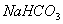 都是盐,都能与溶液反应
都是盐,都能与溶液反应
C.  和
和 都是大气污染物,在空气中都能稳定存在
都是大气污染物,在空气中都能稳定存在
D. Al在浓盐酸中会“钝化”,能用铝槽盛放浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素Q、R、T、W在元素周期表中的位置如图所示,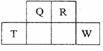 其中T所处的周期序数与主族序数相等。
其中T所处的周期序数与主族序数相等。
(1)T的原子结构示意图是_______。用化学方程式表示冶炼T单质常用原理是________。
(2)与同主族的某元素,其氢氧化物分子含有18个电子,该分子中存在的共价键的类型是___________。
(3)元素的非金属性:Q___W(填“强于”或“弱于”),用方程式简述其理由______。
(4)甲是R的氧化物,通常状况下呈红棕色。现有一试管甲,欲使元素R全部转化为其最高价氧化物对应水化物。实验步骤:将盛有甲的试管倒扣在水槽中,____。
查看答案和解析>>
科目:高中化学 来源: 题型:
合成气(CO和H2为主的混合气体)不但是重要的燃料也是重要的化工原料,制备合成气的方法有多种,用甲烷制备合成气的反应为:
①CH4(g)+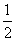 O2(g)====CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
O2(g)====CO(g)+2H2(g) ΔH1=-36 kJ·mol-1
②CH4(g)+H2O(g)====CO(g)+3H2(g) ΔH2=+216 kJ·mol-1
(1)氢气与氧气反应生成水蒸气的热化学方程式为
___________________________________________________________________。
(2)现有1 mol由H2O(g)与O2组成的混合气,且O2的体积分数为x,将此混合气与足量CH4充分反应。
①若x=0.2,反应①放出的能量为________ kJ。
②若x=0.5,反应①与②______(填“放出”或“吸收”)的总能量为_____kJ。
③若x=________时,反应①与②放出(或吸收)的总能量为0。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890 kJ·mol-1
现有H2与CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3 695 kJ,则原混合气体中H2与CH4的物质的量之比是( )
A.1∶1 B.1∶3 C.1∶4 D.2∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com