
 .
. 和CH3COOH(写结构简式).
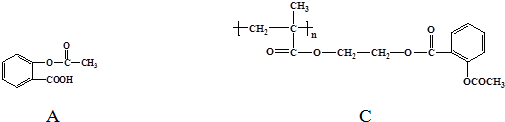
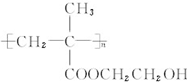
和CH3COOH(写结构简式). 分析 (1)A和B发生酯化反应生成C,根据A、C结构简式确定B结构简式;
(2)A和B发生酯化反应生成C;
(3)A中含有酯基,能发生水解反应生成乙酸和邻羟基苯甲酸.
解答 解:(1)A和B发生酯化反应生成C,根据A、C结构简式确定B结构简式为 ,故答案为:
,故答案为: ;
;
(2)A与B发生酯化反应生成C,反应类型为酯化反应,也属于取代反应,故答案为:酯化反应;
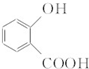
(3)A中含-COOC-,水解生成邻羟基苯甲酸和乙酸,结构简式分别为 、CH3COOH,故答案为:
、CH3COOH,故答案为: ;CH3COOH.
;CH3COOH.
点评 本题考查有机物结构和性质,为高频考点,涉及官能团与性质、有机反应、高分子化合物结构等知识点,明确官能团及其性质关系是解本题关键,知道酯发生水解反应时其断键位置,题目难度不大.


 小学课堂作业系列答案
小学课堂作业系列答案 金博士一点全通系列答案
金博士一点全通系列答案科目:高中化学 来源: 题型:选择题
| A. | 以X浓度变化表示的反应速率为0.01 mol/(L•s) | |
| B. | 将容器体积变为20L,Z的平衡浓度为原来的1/2 | |
| C. | 若增大压强,则物质Y的转化率减小 | |
| D. | 若升高温度,X的体积分数增大,则该反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对于反应nA(g)+B(g)?2C(g),平衡后增大压强,A的百分含量减小,则n≥2 | |
| B. | 对于反应2A(g)?B(g)△H<0,恒温恒容,压强不再变化说明反应达到平衡状态 | |
| C. | 对于反应2A(g)?B(g),恒温恒容条件下,气体密度不变,说明达到平衡状态 | |
| D. | 对于反应2A(g)?B(g),若v(A)正=2v(B)逆,说明反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含氮、磷的化合物 | B. | 含氯的化合物 | C. | 含硫的化合物 | D. | 含碳的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入甲基橙显红色的溶液中:Mg2+、Fe2+、Cl-、NO3- | |
| B. | pH=12的无色透明溶液中:Mg2+、SO42-、NO3-、K+ | |
| C. | 无色透明溶液中:SO42-、NO3-、Na+、Fe3+ | |
| D. | 澄清透明溶液中:Cu2+、SO42-、K+、Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学兴趣小组为了探究某些气体的性质,设计了如图所示的实验装置.实验时将A、D中产生的气体同时通入C中.(K为止水夹,部分夹持仪器已略去)
某化学兴趣小组为了探究某些气体的性质,设计了如图所示的实验装置.实验时将A、D中产生的气体同时通入C中.(K为止水夹,部分夹持仪器已略去)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 石蕊试液 | 品红溶液 | 饱和硫化氢溶液 | 氯水 | |
| A | 无色 | 无色 | 乳白色浑浊 | 无色 |
| B | 红色 | 无色 | 黄色浑浊 | 无色 |
| C | 红色 | 无色 | 乳白色浑浊 | 黄绿色 |
| D | 无色 | 无色 | 乳白色浑浊 | 黄绿色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com