
| A. |  向容量瓶中转移液体 | B. |  向试管内滴加液体 | ||
| C. | 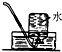 氨气的收集 | D. | 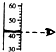 量取液体时读数 |
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②④ | C. | ③⑤ | D. | ④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C与15N有相同的中子数 | B. | 15N与14N互为同位素 | ||
| C. | 13C与C60互为同素异形体 | D. | 15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥⑧ | B. | ②⑥⑧ | C. | ①③④⑦⑧ | D. | ①③④⑤⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 熔点(℃) | 沸点(℃) | 密度(g•cm-3) | 水中溶解度 |
| 甲 | -98 | 57.5 | 0.93 | 可溶 |
| 乙 | -84 | 77 | 0.90 | 可溶 |
| A. | 蒸馏法 | B. | 升华法 | C. | 萃取法 | D. | 过滤法 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
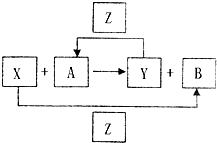 X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可).
X、Y、Z为三种常见的单质,Z为绿色植物光合作用后的产物之一,A、B为常见的化合物.它们在一定条件下可以发生如图所示的转化关系(均不是在溶液中进行的反应)以下每空中填入一种即可).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
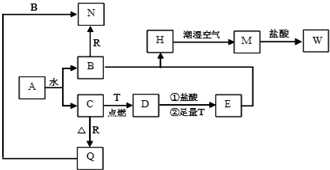
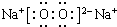 ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com