
| 1000ρω |
| M |
| m |
| ρ |
| 1000×1.84×98% |
| 98 |
| 500mL×1mol/L |
| 18.4mol/L |
| 500mL×1mol/L |
| 18.4mol/L |
| 80g |
| 1g/mL |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
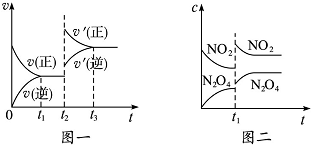
| A、图一t2时改变的条件可能是升高了温度或增大了压强 |
| B、图一t2时改变的条件一定是增大了反应物的浓度 |
| C、图二t1时改变的条件可能是升高了温度或增大了压强 |
| D、若图二t1时改变的条件是增大压强,则混合气体的平均相对分子质量将减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、重结晶提纯KNO3产品除去NaCl时,应在较高温度下溶解产品配成浓溶液后冷却结晶 |
| B、用移液管移取溶液后放入锥形瓶中时,移液管下端不能接触到瓶壁 |
| C、拆卸加热装置、并有导管伸入液体中的,应先停止加热,再将导管取出液面 |
| D、用排水法收集气体时,应将导管伸入集气瓶底部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g)+Cl2(g)=2HCl(g) |
| B、氢气和氯气反应生成 2mol 氯化氢气体,反应的△H=183kJ/mol |
| C、氢气和氯气反应生成 2mol 氯化氢气体,反应的△H=-183kJ/mol |
| D、氢气和氯气反应生成 1mol 氯化氢气体,反应的△H=-183kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、300 mL 3.5 mol/L KCl溶液 |
| B、1 000 mL 2.5 mol/L NaCl溶液 |
| C、250 mL 1 mol/L AlCl3溶液 |
| D、200 mL 2 mol/L MgCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含NaOH 0.1mol |
| B、c(Na+)为1mol/L |
| C、含NaOH 4g |
| D、c(OH-)为0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从1 L 1 mol/L的NaCl溶液中取出100 mL,其浓度为0.1 mol/L |
| B、配制0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L |
| C、0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10 g 98%的硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com