
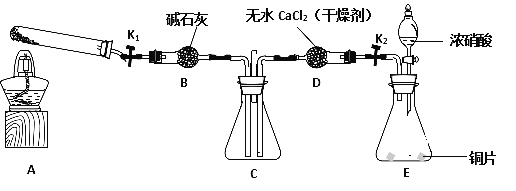
【题目】某兴趣小组的同学发现将一定量的铁与浓硫酸加热时,观察到铁完全溶解,并产生大量气体。为此,他们设计了如下装置验证所产生的气体成分。

(1)填写装置的作用:B___________,C___________,G___________。
(2)证明有S02生成的实验现象是_____________________。
(3)可以证明所产生的气体中含有H2的实验现象是:E中:___________,F中:_________。如果去掉装置D,还能否根据F中的现象判断气体中有H2?_________(填能”或“不能”),原因是_________________________。
(4)反应后A的溶液中含有Fe3+和Fe2+,检验其中Fe2+的方法是____________。
(5)若将铁丝换成铜丝,反应后的溶液没有出现预计的蓝色溶液,而出现了大量白色固体。原因是___________________________;要确认有CuSO4生成,待试管冷却后,____________。写出铜与浓硫酸反应的离子方程式________________________。
【答案】 防止倒吸 检验并吸收SO2 防止空气中的H2O进入F C中酸性高锰酸钾溶液颜色变浅 黑色CuO变成红色Cu 白色无水硫酸铜粉末变成蓝色 不能 因为混合气体中可能含H2O,会干扰H2的检验 取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+ 浓硫酸中的水很少,浓硫酸有吸水性 将浓硫酸倒出,在固体中加水 Cu+2H2SO4![]() Cu2++SO2↑+2H2O+SO42-
Cu2++SO2↑+2H2O+SO42-
【解析】(1)装置B为安全瓶,防止倒吸;C中放置酸性高锰酸钾溶液,检验并除去反应产生的二氧化硫气体;G中放置碱石灰,能够防止空气中的H2O进入F 装置内,影响实验;正确答案:防止倒吸;检验并吸收SO2 ; 防止空气中的H2O进入F。
(2)S02能够与酸性高锰酸钾溶液反应,当C中酸性高锰酸钾溶液颜色变浅时,证明有S02生成;正确答案:C中酸性高锰酸钾溶液颜色变浅。
(3)装置E中试剂为氧化铜粉末,装置F中为无水硫酸铜粉末,H2能够氧化铜发生置换反应生成铜和水,因此反应现象为黑色CuO变成红色Cu , 白色无水硫酸铜粉末变成蓝色;装置D中有浓硫酸,能够吸收水蒸气,如果去掉装置D,就不能根据F中的现象判断气体中有H2,因为混合气体中可能含H2O,会干扰H2的检验;正确答案:黑色CuO变成红色Cu ; 白色无水硫酸铜粉末变成蓝色;不能;因为混合气体中可能含H2O,会干扰H2的检验 。
(4)Fe2+还原性较强,能够使酸性高锰酸钾溶液褪色,而Fe3+不能使酸性高锰酸钾溶液褪色;反应后A的溶液中含有Fe3+和Fe2+,若要检验Fe2+,方法为取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+;正确答案:取A的溶液,滴加酸性高锰酸钾溶液,若红色褪去,证明有Fe2+。
(5)铜丝与浓硫酸加热反应生成硫酸铜,由于浓硫酸中的水很少,浓硫酸有吸水性,所以导致反应后出现了大量白色固体硫酸铜,而不是蓝色硫酸铜溶液;要确认有CuSO4生成,待试管冷却后,将浓硫酸倒出,把固体加入水中,变为蓝色溶液,即可得证;铜与浓硫酸反应生成硫酸铜、二氧化硫和水,离子方程式Cu+2H2SO4![]() Cu2++SO2↑+2H2O+SO42-;正确答案:浓硫酸中的水很少,浓硫酸有吸水性;将浓硫酸倒出,在固体中加水;Cu+2H2SO4
Cu2++SO2↑+2H2O+SO42-;正确答案:浓硫酸中的水很少,浓硫酸有吸水性;将浓硫酸倒出,在固体中加水;Cu+2H2SO4![]() Cu2++SO2↑+2H2O+SO42- 。
Cu2++SO2↑+2H2O+SO42- 。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某化学课外活动小组通过实验研究NO2的性质。
已知:2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O
利用下图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
(1)E装置中制取NO2反应的化学方程式是________________________________。
(2)制取氨气时若只用一种试剂,从下列固体物质中选取___________
a.NH4HCO3 b.NH4C1 c.Ca(OH)2 d.NaOH
(3)若NO2能够被NH3还原,预期观察到C装置中的现象是____________________。
(4)实验过程中气密性良好,但未能观察到C装置中的预期现象。该小组同学从反应原理的角度分析了原因,认为可能是:
① NH3还原性较弱,不能将NO2还原;② 在此条件下,NO2的转化率极低;
③_______________________________________
(5)此实验装置存在一个明显的缺陷是________________________
(6)为了验证NO2能被Na2O2氧化,该小组同学选用B、D、E装置,将B中的药品更换为Na2O2,另选F装置(如右图所示),重新组装,进行实验。
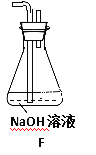
① 装置的合理连接顺序是 _____________
② 实验过程中,B装置中淡黄色粉末逐渐变成白色。经检验,该白色物质为纯净物,且无其他物质生成。推测B装置中反应的化学方程式为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
(1)硅是无机非金属材料的主角。请举出一种含硅元素的材料名称:__________。
(2)可以用浓氨水来检验氯气管道是否漏气,用此方法检查观察到的现象是___________。
(3)某校环保兴趣小组在处理污水样品时,需将质量分数为37%的浓盐酸(密度为1.19g·cm-3)配制成250mL0.1mol·L-1的盐酸。

①在上图所示仪器中,配制上述溶原不需要的是________(填字母)。除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_______________。
②若配制时其他操作均正确,烧杯没有洗涤,则所配溶液的物质的量浓度_________(填“偏高”,“偏低”或“无影响”,下同);定容时俯视,则所配溶液的物质的量浓度_______。
(4)铝制品表面因有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏。若将氧化铝与氢氧化钠的溶液作用,反应的离子方程式为______________________。
(5)工业上用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,最好选用的试剂组合是__________(填字母)。
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的盐酸跟过量的锌粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
A.NaNO3 (溶液)
B.CH3COONa(固体)
C.Na2CO3(溶液)
D.CuSO4 (固体)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】营养强化剂是为了食物的营养价值而强制添加的物质,比如食盐中加碘,是为了预防碘缺乏病的发生。食盐中加碘,所加“碘”指的是( )
A.碘单质B.碘酸钾
C.碘化钾D.次碘酸钾
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g/mL),所得溶液的密度为ρ g/mL,质量分数为ω,物质的量浓度为c mol/L,则下列关系中不正确的是( )
A. ρ=(17V+22 400)/(22.4+22.4V)
B. ω=17c/(1 000ρ)
C. ω=17V/(17V+22 400)
D. c=1 000Vρ/(17V+22 400)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2、CH4、N2O等气体都是“温室气体”.下列有关说法正确的是( )
A.CO2是一种混合物
B.CH4是一种无机物
C.N2O是由N2与O2组成的混合物
D.CO2是由C元素和O元素组成的纯净物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com