
每年夏季,农民焚烧植物秸秆(主要成分是纤维素),既污染了环境,又浪费了资源,工业上以植物秸秆为原料合成某聚酯化合物的路线如下:
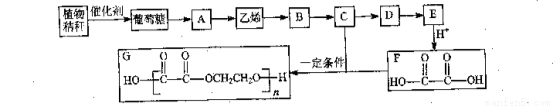
已知A是常见的消毒剂,又可作为能源。
(1)乙烯中官能团的结构式为___________;葡萄糖分子中官能团的电子式为_______________;
(2)由B转化为C的反应条件是________________;C转化为D的反应类型是___________;
(3)测定D中所含官能团的物理方法是__________;若B是氯代烃,其系统命名法的名称是_______;
(4)写出下列反应方程式:
A:由植物秸秆转化成葡萄糖________________________________________________;
B:由A转化成乙烯__________________________________________________;
C:生成聚酯化合物__________________________________________________。
(1)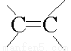 ( 1分);
( 1分);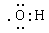 ( 1分),
( 1分),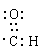 (1分)
(1分)
(2)NaOH水溶液,加热 1分;氧化反应 (1分) (3)红外光谱 2分;1、2—二氯乙烷 (2分)
(4)A:(C6H10O5)n+nH2O 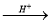 nC6H12O6 (2分)
nC6H12O6 (2分)
淀粉 葡萄糖
B:CH3CH2OH CH2=CH2↑+H2O (2分)
CH2=CH2↑+H2O (2分)
C :nHOCH2CH2OH+nHOOC-COOH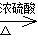
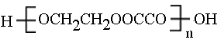 +(2n-1)H2O (2分)
+(2n-1)H2O (2分)
【解析】
试题分析:(1)乙烯属于烯烃,分子中的官能团是碳碳双键,其结构式为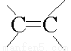 ;葡萄糖分子中官能团的官能团是羟基和醛基,其电子式分别为
;葡萄糖分子中官能团的官能团是羟基和醛基,其电子式分别为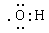 、
、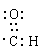 ;
;
(2)葡萄糖在一定条件下分解生成CO2和乙醇,由于A可以转化为乙烯,所以A是乙醇。F和C发生缩聚反应生成G,则根据二者的结构简式可知,C应该是乙二醇,因此B应该是1,2-二氯乙烷,则由B转化为C的反应条件是氢氧化钠溶液加热;乙二醇发生氧化反应生成乙二醛,乙二醛继续氧化后酸化转化为乙二酸,则C转化为D的反应类型是氧化反应;
(3)测定D中所含官能团的物理方法是红外光谱;若B是氯代烃,其系统命名法的名称是1,2-二氯乙烷;
(4)A:由植物秸秆转化成葡萄糖属于淀粉的水解,化学方程式为(C6H10O5)n+nH2O 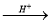 nC6H12O6 ;
nC6H12O6 ;
淀粉 葡萄糖
B:乙醇发生消去反应生成乙烯,则由A转化成乙烯的化学方程式为CH3CH2OH CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
C:乙二醇与乙二酸通过缩聚反应生成高分子化合物,则生成聚酯化合物的化学方程式为nHOCH2CH2OH+nHOOC-COOH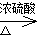
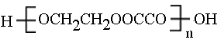 +(2n-1)H2O。
+(2n-1)H2O。
考点:考查有机物推断、官能团、有机反应类型以及方程式的书写等


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源:2013-2014四川省眉山市高三第二次诊断性考试理综化学试卷(解析版) 题型:选择题
化学与生活密切相关,下列说法正确的是
A.医药中常用酒精消毒是因为酒精能够使细菌蛋白体发生盐析
B.开发清洁能源汽车(如太阳能汽车等)能减少或控制汽车尾气污染
C.目前废旧电池的回收,主要是为了防止电池中NH4Cl对水资源的污染
D.为了防止中秋月饼等富脂食品氧化变质,可在包装袋中放入生石灰
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市高第二期期末高一化学试卷(解析版) 题型:填空题
工业上用含有铝、铁、铜的废弃合金为主要原料制取硫酸铝溶液、硝酸铜晶体和无水氯化铁,其生产流程如下图所示。
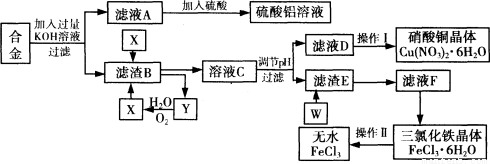
已知:调节适当PH范围可使Fe3+沉淀完全而Cu2+不会沉淀。
请回答下列问题:
(1)写出向合金中加入KOH溶液后所发生反应的离子方程式: 。
(2)在滤液A中直接加入硫酸后所得到的硫酸铝溶液中除含少量硫酸外,还一定含有的杂质是
(填化学式)。
请设计一个更合理的实验方案由滤液A制备纯净的硫酸铝溶液,仿照上图形式画出制备流程图(提示:在箭头上下方标出所用试剂和实验操作) 。
(3) 写出试剂X的名称 。
(4) 实验操作I的顺序依次为 (选填序号)。
A.蒸馏 B.蒸发浓缩 C.过滤 D.冷却结晶
(5) 要制得更纯的Cu(NO3)2·6H2O晶体,必须进行的操作是 (填操作名称)
(6)写出滤渣E与W反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市高第二期期末高一化学试卷(解析版) 题型:选择题
下列离子方程式或化学方程式书写正确的是 ( )
A.实验室用氯化铵与消石灰制氨气 NH4++OH- NH3↑+H2O
NH3↑+H2O
B.将CO2通入BaCl2溶液中 H2O +CO2+Ba2+ =BaCO3↓+2H+
C.少量SO2通入加漂白粉的水溶液中 SO2+H2O+Ca2++3ClO- = CaSO4↓+2HClO+Cl-
D.用H2还原MgO H2+MgO  Mg+H2O
Mg+H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市高第二期期末高一化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列叙述不正确的是( )
A.7.80g Na2O2与5.85g NaCl所含阴离子数均为0.1NA
B.常温常压下,22.4LNH3所含分子数小于NA
C. 一定条件下,1.4g N2与0.2mol H2混合充分反应,转移的电子数为0.3NA
D.标准状况下,28g聚乙烯完全燃烧,产生的CO2数为2NA
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市五校高二下学期期中联考化学试卷(解析版) 题型:选择题
氯原子对O3的分解有催化作用:O3+Cl=ClO+O2 ΔH1,ClO+O=Cl+O2 ΔH2。大气臭氧层的分解反应是:O3+O=2O2 ΔH,该反应的能量变化如图所示,则下列叙述正确的是( )。
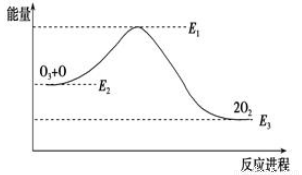
①反应O3+O=2O2的ΔH=E1-E3 ②反应O3+O=2O2是放热反应 ③ΔH=ΔH1+ΔH2 ④大气层中的臭氧无法再生
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市五校高一下学期期中联考化学试卷(解析版) 题型:简答题
(14分)元素周期表是学习化学的重要工具,它隐含着许多信息和规律,下面是八种短周期元素的相关信息(已知铍的原子半径为0.089nm)
元素代号 | A | B | C | D | E |
原子半径/nm | 0.16 | 0.143 | 0.102 | 0.099 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | -1 | -2 |
F原子中无中子,G最高正价数与负价数相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色(用相应的元素符号完成下列空白)
(1)B元素在元素周期表中的位置___________________,上述八种元素的最高价氧化物对应的水化物中酸性最强的是__________,A离子的结构示意图_______________。
(2)用电子式表示A、D形成化合物的过程:____________________________________。H、E形成原子个数比为1:1的化合物的电子式为___________,含有的化学键类型为____________。C2D2的电子式为______________________。
(3)下列说法能说明D的非金属性比C强的选项____________
①H2CO4比HDO稳定②HDO4比H2CO4酸性强③C2-比D-易被氧化④HD比H2C稳定⑤铜与HD不反应,但能与浓H2CO4反应⑥铁与D2加热生成FeD3,铁与C加热生成FeC⑦C原子与D原子电子层数相同,D原子半径小于C原子。
A、全部 B、②③④⑥⑦ C、①②④⑤⑥ D、除①以外
(4)A、B、C、D、E形成的简单离子半径由大到小的顺序为_______________________。(用具体离子符号表示)
(5)C单质与H的最高价氧化物对应水化物在加热条件下能发生反应,若有3mol的C参与反应,转移4NA的电子,请写出离子反应方程_______________________________________,氧化剂与还原剂的质量之比_____________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省成都市五校高一下学期期中联考化学试卷(解析版) 题型:选择题
下列电子式书写正确的是 ( )
A.氮气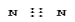 B.二氧化碳
B.二氧化碳
C.水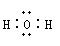 D.氯化铵
D.氯化铵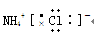
查看答案和解析>>
科目:高中化学 来源:2013-2014四川省高三5月冲刺卷理综化学试卷(解析版) 题型:选择题
已知A、B、C、D、E是短周期中原子序数依次增大的5种元素,A在反应中既不容易得电子也不容易失电子,元素B的最外层电子数是电子层数的3倍,元素D与A为同族元素,元素C和E形成的化合物CE是海水中的主要成分。下列说法不正确的是
A.离子半径:r(E)>r(B)>r(C)
B.熔点:CE>DE4
C.C与B形成的两种化合物中化学键类型不同
D.A、D、E的最高价氧化物对应水化物的酸性逐渐增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com