
 ÓŠX”¢Z”¢WČżÖÖŗ¬14øöµē×ÓµÄĮ£×Ó£¬Ęä½į¹¹ĢŲµćČēĻĀ£ŗ
ÓŠX”¢Z”¢WČżÖÖŗ¬14øöµē×ÓµÄĮ£×Ó£¬Ęä½į¹¹ĢŲµćČēĻĀ£ŗ| Į£×Ó“śĀė | X | Z | W |
| Ō×ÓŗĖŹżÄæ | µ„ŗĖ | Ķ¬ÖÖŌŖĖŲ¹¹³ÉµÄĮ½ŗĖ | Ķ¬ÖÖŌŖĖŲ¹¹³ÉµÄĮ½ŗĖ |
| Į£×ӵĵēŠŌ | µēÖŠŠŌ | Į½øöµ„Ī»øŗµēŗÉ | µēÖŠŠŌ |
·ÖĪö X”¢Z”¢WČżÖÖŗ¬14øöµē×ÓµÄĮ£×Ó£¬XĪŖµ„ŗĖ£¬µēÖŠŠŌ£¬¹ŹXµÄÖŹ×ÓŹżĪŖ14£¬XĪŖSiŌ×Ó£»ZĪŖĶ¬ŌŖĖŲ¹¹³ÉµÄĮ½ŗĖĮ£×Ó£¬Į½øöµ„Ī»øŗµēŗÉ£¬¹ŹŠĪ³ÉZŌŖĖŲµÄŌ×ÓÖŹ×ÓŹżĪŖ$\frac{14-2}{2}$=6£¬¹ŹZĪŖC22-£»WĪŖĶ¬ŌŖĖŲ¹¹³ÉµÄĮ½ŗĖĮ£×Ó£¬µēÖŠŠŌ£¬¹ŹŠĪ³ÉWŌŖĖŲµÄŌ×ÓÖŹ×ÓŹżĪŖ$\frac{14}{2}$=7£¬ĪŖNŌŖĖŲ£¬WĪŖN2£¬MŌ×ÓŗĖĶā±ČXŌÓ趹2øöµē×Ó£¬ŌņMĪŖS£¬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗX”¢Z”¢WČżÖÖŗ¬14øöµē×ÓµÄĮ£×Ó£¬XĪŖµ„ŗĖ£¬µēÖŠŠŌ£¬¹ŹXµÄÖŹ×ÓŹżĪŖ14£¬XĪŖSiŌ×Ó£»ZĪŖĶ¬ŌŖĖŲ¹¹³ÉµÄĮ½ŗĖĮ£×Ó£¬Į½øöµ„Ī»øŗµēŗÉ£¬¹ŹŠĪ³ÉZŌŖĖŲµÄŌ×ÓÖŹ×ÓŹżĪŖ$\frac{14-2}{2}$=6£¬¹ŹZĪŖC22-£»WĪŖĶ¬ŌŖĖŲ¹¹³ÉµÄĮ½ŗĖĮ£×Ó£¬µēÖŠŠŌ£¬¹ŹŠĪ³ÉWŌŖĖŲµÄŌ×ÓÖŹ×ÓŹżĪŖ$\frac{14}{2}$=7£¬ĪŖNŌŖĖŲ£¬WĪŖN2£¬MŌ×ÓŗĖĶā±ČXŌÓ趹2øöµē×Ó£¬ŌņMĪŖS£¬
£Ø1£©XµÄŃõ»ÆĪļĪŖ¶žŃõ»Æ¹č£¬¶žŃõ»Æ¹č¾§ĢåÖŠŗ¬ÓŠ»Æѧ¼üĄąŠĶŹĒ¹²¼Ū¼ü£¬
¹Ź“š°øĪŖ£ŗ¹²¼Ū¼ü£»
£Ø2£©ZĪŖC22-£¬ZÓėøĘĄė×Ó×é³ÉµÄ»ÆĢØĪļµÄµē×ÓŹ½ĪŖ Ca2+[C??C]2-£¬
¹Ź“š°øĪŖ£ŗCa2+[C??C]2-£»
£Ø3£©WĪŖN2£¬×é³ÉWµÄŌŖĖŲµÄ¼ņµ„Ēā»ÆĪļĪŖ°±Ęų£¬NH3ÓėH2O¼äÄÜŠĪ³ÉĒā¼ü£¬NH3ÓėH2O¶¼ŹĒ¼«ŠŌ·Ö×ÓĒŅĻą»„¼äÄÜ·“Ӧɜ³ÉŅ»Ė®ŗĻ°±£¬ĖłŅŌ°±Ęų¼«Ņ×ČÜÓŚĖ®£¬°±ĘųÓėæÕĘųæÉŅŌ¹¹³ÉŅ»ÖÖČ¼ĮĻµē³Ų£¬²śĪļĪŖĪŽ¶¾ĪļÖŹÓ¦ĪŖµŖĘųŗĶĖ®£¬µē½āÖŹČÜŅŗŹĒKOHČÜŅŗ£¬øƵē³ŲÖŠ°±ĘųŹĒ»¹Ō¼Į£¬ŌŚøŗ¼«·¢ÉśŃõ»Æ·“Ó¦£¬µē¼«·“Ó¦Ź½ĪŖ 2NH3-6e-+6OH-ØTN2+6H2O£¬øł¾Żµē¼«·“Ó¦Ź½æÉÖŖ£¬Ļūŗıź×¼×“æöĻĀ1.12L¼“0.05mol°±ĘųŹ±£¬×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ0.15mol£¬µē½ā1.5L 1mol/LNaClČÜŅŗ£¬Éś³É0.15molĒāŃõ»ÆÄĘ£¬ČÜŅŗÖŠĒāŃõøłµÄÅضČĪŖ$\frac{0.15mol}{1.5L}$=0.1mol/L£¬ĖłŅŌČÜŅŗµÄpH=13£¬
¹Ź“š°øĪŖ£ŗNH3ÓėH2O¼äÄÜŠĪ³ÉĒā¼ü£¬NH3ÓėH2O¶¼ŹĒ¼«ŠŌ·Ö×ÓĒŅĻą»„¼äÄÜ·“Ӧɜ³ÉŅ»Ė®ŗĻ°±£»2NH3-6e-+6OH-ØTN2+6H2O£»13£»
£Ø4£©æÉÄę·“Ó¦2SO2£ØĘų£©+O2£ØĘų£©?2SO3£ØĘų£©ŌŚĮ½øöĆܱÕČŻĘ÷ÖŠ½ųŠŠ£¬AČŻĘ÷ÖŠÓŠŅ»øöæÉÉĻĻĀŅĘ¶ÆµÄ»īČū£¬BČŻĘ÷æɱ£³ÖŗćČŻ£¬ČōŌŚA”¢BÖŠ·Ö±š³äČė1molO2ŗĶ2mol SO2£¬Ź¹ĘųĢåĢå»żV£ØA£©=V£ØB£©£¬ŌŚĻąĶ¬ĪĀ¶ČĻĀ·“Ó¦£¬ÓÉÓŚøĆ·“Ó¦ĪŖĘųĢåĢå»ż¼õŠ”µÄ·“Ó¦£¬ĖłŅŌAČŻĘ÷ÖŠµÄŃ¹Ēæ“óÓŚBČŻĘ÷£¬ĖłŅŌt£ØA£©t£¼£ØB£©Ę½ŗāŹ±SO2µÄ×Ŗ»ÆĀŹ£ŗa£ØA£©£¾a£ØB£©£¬
¹Ź“š°øĪŖ£ŗ£¼£»£¾£»
£Ø5£©±Č½ĻSiŗĶSĮ½ŌŖĖŲµÄ·Ē½šŹōŠŌĻą¶ŌĒæČõ£¬æÉŅŌøł¾ŻĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ”¢µ„ÖŹÓėĒāĘų»ÆŗĻµÄÄŃŅץ“ÅŠ¶Ļ£¬¶ų²»ÄÜøł¾ŻĘųĢ¬Ēā»ÆĪļµÄ·Šµć¼°µ„ÖŹŌŚ³£ĪĀĻĀµÄדĢ¬ÅŠ¶Ļ£¬¹ŹŃ”c”¢d£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲ»ÆŗĻĪļĶʶĻ”¢³£ÓĆ»ÆѧÓĆÓļ”¢µē¼«·“Ó¦”¢Ó°Ļģ»ÆŃ§Ę½ŗāŅĘ¶ÆµÄŅņĖŲ”¢ŌŖĖŲÖÜĘŚĀÉµČ£¬ÄѶČÖŠµČ£¬×¢Ņā»ł“”ÖŖŹ¶µÄĮé»īŌĖÓĆ£®


 µ¼Ń§Óė²āŹŌĻµĮŠ“š°ø
µ¼Ń§Óė²āŹŌĻµĮŠ“š°ø ŠĀ·Ē·²½Ģøسå“Ģ100·ÖĻµĮŠ“š°ø
ŠĀ·Ē·²½Ģøسå“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ü£¾¢Ū£¾¢Ś£¾¢Ł | B£® | ¢Ū£¾¢Ü£¾¢Ś£¾¢Ł | C£® | ¢Ś£¾¢Ū£¾¢Ü£¾¢Ł | D£® | ¢Ū£¾¢Ś£¾¢Ü£¾¢Ł |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na2OČÜÓŚĖ®£ŗNa2O+H2O=2Na++2OH- | |
| B£® | ĻņCa£ØClO£©2ČÜŅŗÖŠĶØČė¹żĮæCO2£ŗ2ClO-+H2O+CO2=2HClO+CO32- | |
| C£® | ÓĆFeCl3ČÜŅŗøÆŹ“Ķ°å£ŗFe3++Cu=Fe2++Cu2+ | |
| D£® | Ģ¼ĖįøĘČÜÓŚĻ”“×Ėį£ŗCaCO3+2H+=Ca2++CO2”ü+H2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  | B£® | C3H6 | C£® |  | D£® | CH2CHCH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
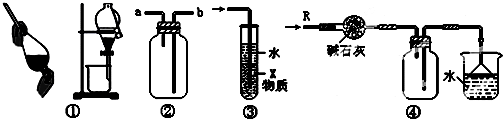
| A£® | ×°ÖĆ¢ŁæÉÓĆÓŚ·ÖĄėŅŅ“¼ŗĶĖ®µÄ»ģŗĻĪļ | |
| B£® | ×°ÖĆ¢ŚæÉÓĆÓŚŹÕ¼ÆH2”¢NH3”¢CO2”¢Cl2”¢HCl”¢NO2µČĘųĢå | |
| C£® | ×°ÖĆ¢ŪÖŠXČōĪŖĖÄĀČ»ÆĢ¼£¬æÉÓĆÓŚĪüŹÕ°±Ęų»ņĀČ»ÆĒā£¬²¢·ĄÖ¹µ¹Īü | |
| D£® | ×°ÖĆ¢ÜæÉÓĆÓŚøÉŌļ”¢ŹÕ¼Æ°±Ęų£¬²¢ĪüŹÕ¶ąÓąµÄ°±Ęų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | “ņæŖĘ”¾ĘĘæøĒ£¬²śÉś“óĮæĘųÅŻ | |
| B£® | Ļ”ŹĶCH3COOHŹ±£¬ČÜŅŗÖŠCH3COO-ŹżÄæŌö¶ą | |
| C£® | ¹¤ŅµŗĻ³É°±³£ÓĆ500”ę×óÓŅµÄĪĀ¶Č | |
| D£® | Čȵēæ¼īČÜŅŗµÄČ„ĪŪŠ§¹ū±ČĄäµÄŗĆ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NAøöČĪŗĪĘųĢå·Ö×ÓĖłÕ¼Ģå»ż¶¼Ō¼ŹĒ22.4L | |
| B£® | NAøöH3O+ŗ¬ÓŠµē×ÓŹżÄæĪŖ11NA | |
| C£® | 0.5mol/L NaOHČÜŅŗÖŠŗ¬ÓŠ0.5NAøöNa+ | |
| D£® | NAøöCO2ŗĶNO2µÄ»ģŗĻĘųĢåÖŠŃõŌ×ÓŹżÄæĪŖ2NA |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com