
选择合适的试剂除去杂质(括号内为杂质),并写出发生的反应的离子方程式
(1)CO2(HCl)试剂 ,离子方程式
(2)Na2CO3溶液(NaHCO3)试剂 ,离子方程式
(3)FeCl3 溶液(FeCl2)试剂 ,离子方程式
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH > a,则该电解质可能是( )
A.NaOH B.H2SO4 C.AgNO3 D.Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关氧化还原反应的叙述中正确的是
A.有单质参加或有单质生成的反应一定是氧化还原反应
B.金属单质在化学反应中一定作还原剂
C.失电子的反应物在反应中作氧化剂,反应中被还原
D.氧化还原的本质是元素化合价的升降
查看答案和解析>>
科目:高中化学 来源: 题型:
固体单质A和气体单质B在容积一定的密闭容器中恰好完全反应生成气体C,相同温度下测得容器内压强不变,若产物气体C的密度是原气体密度的4倍,则判断正确的是
A. 单质A、B的摩尔质量之比是1∶4
B. 反应前后的气体质量之比一定是1∶4
C. 生成物C中,A的质量分数为50%
D. 生成物C中A、B两元素的原子个数比为3:1
查看答案和解析>>
科目:高中化学 来源: 题型:
把500mLNH4HCO3和Na2CO3的混合溶液分成五等份,取一份加入含amol氢氧化钠的溶液恰好反应完全;另取一份加入含b mol HCl的盐酸恰好反应完全,则该混合溶液中c(Na+)为
A.( )mol/L B.( 2b—a ) mol/L
)mol/L B.( 2b—a ) mol/L
C.( l0b - 5a) mol/L D.(5b一2.5a)mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
将等物质的量浓度的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液pH随时间t变化的曲线如右图,则下列说法正确的是( )
A.阳极产物一定是Cl2,阴极产物一定是Cu
B.BC段表示在阴极上是H+放电产生了H2
C.整个过程中阳极先产生Cl2,后产生O2
D.CD段表示阳极上OH一放电破坏了水的电离平衡,产生了H+

查看答案和解析>>
科目:高中化学 来源: 题型:
如图,A池用石墨电极电解NaOH溶液,B池精炼粗铜,一段时间后停止通电,A池中d极产生具有氧化性的气体在标准状况下为2.24L。下列说法正确的是( )
A.A池为电解池,B池为原电池
B.两池中d、e两极都发生氧化反应
C.B池中e极应为粗铜板材料
D.B池中e极质量增加12.8g

查看答案和解析>>
科目:高中化学 来源: 题型:
要除去碳酸氢钠溶液中混有的少量碳酸钠,最好采用
A.加入过量的澄清石灰水 B.加入适量的氢氧化钠溶液
C.将溶液加热蒸干并灼烧 D.通入足量的CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
“低碳循环”已经引起了国民的重视,试回答下列问题:
(1)煤的气化和液化可以提高燃料的利用率。
已知25℃,101 时:
时:

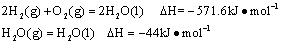
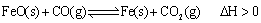 则在25℃,101
则在25℃,101 时:
时: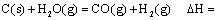 .
.
(2)高炉炼铁是CO气体的重要用途之一,其基本反应为:
已知在1100℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值 (填“增大”、“减小”或“不变”);
②1100℃时测得高炉时, ,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是 。
,在这种情况下,该反应是否处于化学平衡状态? (填“是”或“否”),其判断依据是 。
③目前工业上可用 来生产燃料甲醇,有关反应为:
来生产燃料甲醇,有关反应为:
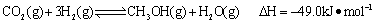 。现向体积为1L的密闭容器中,充入1mol
。现向体积为1L的密闭容器中,充入1mol 和3mol
和3mol ,反应过程中测得
,反应过程中测得 和
和 (g)的浓度随时间的变化如图所示。
(g)的浓度随时间的变化如图所示。
Ⅰ、从反应开始到平衡,氢气的平均反应速率 ;
;
Ⅱ、下列措施能使 增大的是 (填符号)。
增大的是 (填符号)。
 A.升高温度 B.再充入
A.升高温度 B.再充入
C.再充入 D.将
D.将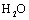 (g)从体系中分离
(g)从体系中分离
E.充入He(g),使体系压强增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com