
��10�֣����ڳ��о���ʹ�õĹܵ�ú������Ҫ�ɷ���H2��CO������CH4��H2��CO��CH4��ȼ�����������±�
���� | H2 | CO | CH4 |
ȼ����kJ?mol-1 | 285��8 | 283��0 | 890��3 |
��1����д��H2��CO��CH4ȼ�յ��Ȼ�ѧ����ʽ��
�� �� ��
��2����Ϊ�����������������乤�̵���Ҫ�ɾͣ�������Ȼ����ȫ������Ϻ������վ��ڣ�ʹ�ùܵ�ú���û�������Ȼ����Ӧ������߽��������ţ�������_____�������������Ȼ�������Ľ����������_____�������������Ȼ�������Ľ��������ݱ�����ͬʱȼ���۸�Ҳ�������е�0��95Ԫ/m3�Ļ����ϵ�����1��31Ԫ/m3����ͨ������˵������������ˮƽ���䣬������ȼ����������Ѵ�Լ�����ڵ�____��������ȷ��С�����2λ��
��1�� H2(g)+1/2O2(g)=H2O(l) ��H3=��285��8KJ/mol��CO(g)+ 1/2O2(g)= CO2(g) ��H=��283��0KJ/mol ��CH4(g)+2O2(g)= CO2(g)��2H2O(l) ��H=��890��3KJ/mol ����2����������Ȼ����0��44��
��������
�����������1�����ݱ��������ʵ�ȼ���ȵ���ֵ��֪��H2��CO��CH4ȼ�յ��Ȼ�ѧ����ʽ�ǣ�1�� H2(g)+1/2O2(g)=H2O(l) ��H3=��285��8KJ/mol��CO(g)+ 1/2O2(g)= CO2(g) ��H=��283��0KJ/mol ��CH4(g)+2O2(g)= CO2(g)��2H2O(l) ��H=��890��3KJ/mol ����2����Ϊ�����������������乤�̵���Ҫ�ɾͣ�������Ȼ����ȫ������Ϻ������վ��ڣ�ʹ�ùܵ�ú���û�������Ȼ�������ڵ�λ�������Ȼ�����ĵ�������������Ӧ������߽��������ţ�����������Ľ������������Ȼ���Ľ��������ݱ�����ͬʱȼ���۸�Ҳ�������е�0��95Ԫ/m3�Ļ����ϵ�����1��31Ԫ/m3������1mol�Ĺܵ�ú��ȼ�շų������ǣ�283��0+285��8��KJ��2=284��4KJ��1mol����Ȼ���ų�������890��3KJ����������������ˮƽ���䣬�����ĵ��������䣬�����Ҫ������Ȼ�������ʵ�����ú����284��4KJ��890��3KJ=0��32����ԭ������1m3,����0��95Ԫ�������ĵ���Ȼ���������0��32m3,��Ҫ���ѣ�0��32m3��1��31Ԫ/m3=0��42Ԫ������������ȼ����������Ѵ�Լ�����ڵı�����ϵ�ǣ�0��42Ԫ��0��95Ԫ=0��44���������ʸ����á�
���㣺����ȼ���ȵ��Ȼ�ѧ����ʽ����д��ȼ�ղ�ͬȼ�ϵ���ߵĸ��췽�������Ѵ�С�ıȽϵļ��㡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��2015��ӱ�ʡ��һ��һѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
(6��)�±���ij���г������۵�һ�֡��ӵ��Ρ���װ���ϵIJ�������˵��������ݴ˱�����ϳ���ѧ���Ļ�ѧ֪ʶ���ش��������⣺
���ϱ� | ���ƺ��Ρ�����أ�KIO3�� |
������ | 20~40mg/kg |
���ط��� | �ܷ�ܹ⡢���� |
ʹ�÷��� | ���ʱ��ʳƷ��������� |
��1������������������ʣ�______________�������������������������ʡ������������
��2�����ݺ����ε�ʳ�÷��������Ʋ����صĻ�ѧ���ʣ�
�����������ʱ_____________��
��3���ҹ��涨��ʳ�κ�����Ϊÿǧ��ʳ�κ���0��035g���൱��ÿǧ��ʳ�κ�����ء���������g (���������λС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ں��з�̪��0.1 mol��L��1��ˮ�м���������NH4Cl���壬����Һ��ɫ
A������ɫ B������ C����dz D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
������������AG��ʾ��Һ����ȣ�acidity grade����AG�Ķ���ΪAG��lg��c��H+��/c��OH�����ݡ����б�����ȷ����
A����25��ʱ������Һ�����ԣ���pH��7��AG��1
B����25��ʱ������Һ�����ԣ���pH��7��AG��0
C����25��ʱ������Һ�ʼ��ԣ���pH��7��AG��0
D����25��ʱ����Һ��pH��AG�Ļ��㹫ʽΪAG��2��7��pH��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�B�㻯ѧ�Ծ��������棩 ���ͣ������
��7�֣�����ϩΪԭ�Ϻϳɻ�����C������������ʾ��
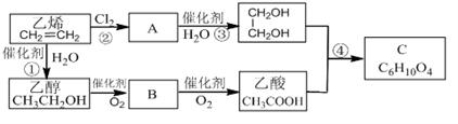
��1�� �Ҵ������������������ŵ����Ʒֱ�Ϊ�� �� ��
��2�� B���ʵĽṹ��ʽΪ ���� ��
��3�� �� ���ܵķ�Ӧ���ͷֱ�Ϊ ��Ӧ�� ��Ӧ��
��4�� ��Ӧ�ںܵ͢Ļ�ѧ����ʽ�ֱ�Ϊ��
�� ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�B�㻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����Ⱥ����ܱ�������ֻͨ��A��g����B��g������һ��������ʹ��ӦA��g��+B��g�� 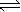 C��g��+D��g���ﵽƽ�⣬��Ӧ����������Ӧ������ʱ��仯��ʾ��ͼ��ͼ��ʾ������˵����ȷ���ǣ� ��
C��g��+D��g���ﵽƽ�⣬��Ӧ����������Ӧ������ʱ��仯��ʾ��ͼ��ͼ��ʾ������˵����ȷ���ǣ� ��
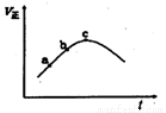
A���÷�Ӧ����ӦΪ���ȷ�Ӧ
B����Ӧ���Ũ�ȣ�a��С��b��
C����Ӧ��c��ﵽƽ��
D����Ӧ�ﵽƽ��ʱ�������¶ȣ��淴Ӧ���ʽ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�B�㻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���� �� ��
A������ѹǿ��ʹ�������Ŀ���ӣ���ѧ��Ӧ����һ������
B�������¶ȣ�ʹ����Ӱٷ������ӣ���ѧ��Ӧ����һ������
C������Ӽ��������ķ��Ӽ����ײ��Ϊ��Ч��ײ
D�����뷴Ӧ�ʹ����Ӱٷ������ӣ���ѧ��Ӧ����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�A�㻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��Ca��OH��2��������ˮ�У�һ��ʱ���ﵽ����ƽ�⣺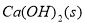
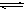
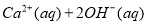 ������˵����ȷ���ǣ�������
������˵����ȷ���ǣ�������
A������������Һ�м�CaO����Һ��pH����
B������Һ���ȣ���Һ��pH����
C������Һ�м���Na2CO3��Һ�����й�����������
D������Һ�м�������NaOH���壬Ca��OH��2������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭����У9�������߶���ѧ�Ծ��������棩 ���ͣ�ѡ����
������̶����ܱ������н��п��淴Ӧ2NO2 2NO+O2����������Ϊ��Ӧ�ﵽƽ��״̬��־����( )
2NO+O2����������Ϊ��Ӧ�ﵽƽ��״̬��־����( )
�ٵ�λʱ��������nmol O2��ͬʱ����2n mol NO2
�ڵ�λʱ��������n mol O2 ��ͬʱ����2n mol NO
����NO2 ��NO��O2��ʾ�ķ�Ӧ����֮��Ϊ2��2��1
�ܻ���������ɫ���ٸı� �ݻ��������ܶȲ��ٸı�
��������ѹǿ���ٸı� ��������ƽ����Է����������ٸı�
A���٢ܢޢ� B���ڢۢݢ� C���٢ۢܢ� D��ȫ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com