
分析 (1)NH3与NaClO反应可得到肼(N2H4),依据氧化还原反应化合价变化分析书写化学方程式:
(2)依据盖斯定律,结合题干热化学方程式计算写出;
(3)原电池反应中负极失电子发生氧化反应;
(4)①已知:Ⅰ、2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g),
Ⅱ、2NO(g)+Cl2(g)?2ClNO(g),
根据盖斯定律①×2-②可得:4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g),则该反应平衡常数为①的平衡常数平方与②的商;
②测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则△n(ClNO)=7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,由方程式计算参加反应NO、氯气的物质的量,进而计算平衡时氯气的物质的量、NO的转化率;正反应为气体物质的量减小的反应,恒温恒容下条件下,到达平衡时压强比起始压强小,其他条件保持不变,反应(Ⅱ)在恒压条件下进行,等效为在恒温恒容下的平衡基础上增大压强,平衡正向移动;平衡常数只受温度影响,温度不变,平衡常数不变.
解答 解:(1)NH3与NaClO反应可得到肼(N2H4),次氯酸钠做氧化剂,依据氧化还原反应的电子守恒和原子守恒写出该反应的化学方程式为:2NH3+NaClO=N2H4+NaCl+H2O;
故答案为:2NH3+NaClO=N2H4+NaCl+H2O;
(2)①N2(g)+2O2(g)=N2O4(l)△H1=-19.5kJ?mol-1
②N2H4(l)+O2 (g)=N2(g)+2H2O(g)△H2=-534.2kJ•mol-1
根据盖斯定律写出肼和N2O4反应的热化学方程:②×2-①得到:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9KJ/mol;
故答案为:2N2H4(l)+N2O4(l)=3N2(g)+4H2O(g)△H=-1048.9KJ/mol;
(3)肼一空气燃料电池是一种碱性电池,该电池放电时,肼失电子被氧化发生负极反应,依据反应②写出负极的反应式为:N2H4+4OH--4e-=4H2O+N2↑;
故答案为:N2H4+4OH--4e-=4H2O+N2↑;
(4)2NO2(g)+NaCl(s)?NaNO3(s)+ClNO(g) K1 △H<0 (I)
2NO(g)+Cl2(g)?2ClNO(g) K2 △H<0 (II)
根据盖斯定律,Ⅰ×2-Ⅱ可得:4NO2(g)+2NaCl(s)?2NaNO3(s)+2NO(g)+Cl2(g),则该反应平衡常数K=K12/K2,故答案为:K12/K2;
②测得10min内v(ClNO)=7.5×10-3mol•L-1•min-1,则△n(ClNO)=7.5×10-3mol•L-1•min-1×10min×2L=0.15mol,
由方程式可知,参加反应氯气的物质的量为0.15mol×$\frac{1}{2}$=0.075mol,故平衡时氯气的物质的量为0.1mol-0.075mol=0.025mol;
参加反应NO物质的量为0.15mol,则NO的转化率为$\frac{0.15mol}{0.2mol}$×100%=75%;正反应为气体物质的量减小的反应,恒温恒容下条件下,到达平衡时压强比起始压强小,其他条件保持不变,反应(Ⅱ)在恒压条件下进行,等效为在恒温恒容下的平衡基础上增大压强,平衡正向移动,NO转化率增大,故转化率α2>α1;平衡常数只受温度影响,温度不变,平衡常数不变,即平衡常数K2 不变,反应释放热量,所以若要使K2减小,可采取的措施是升高温度,
故答案为:0.025;75%;>;不变;升高温度.
点评 本题考查了热化学方程式的书写,盖斯定律的应用,原电池的工作原理应用,电极反应的书写方法、化学平衡计算与影响因素、化学平衡常数等,侧重考查学生分析计算能力,需要学生具备扎实的基础与灵活应用能力,题目难度不大.


科目:高中化学 来源: 题型:选择题
| X溶液 | 现象 |  | |
| A | 稀HNO3酸化的AgNO3溶液 | 有白色沉淀生成 | |
| B | 滴有KSCN的FeSO4溶液 | 溶液变为血红色 | |
| C | 淀粉KI酸性溶液 | 溶液变为蓝色 | |
| D | 紫色石蕊溶液 | 溶液先变红后褪色 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B元素在周期表中的位置为第二周期ⅣA族 | |
| B. | D的氧化物和E的单质的水溶液均有漂白性,且漂白的原理相同 | |
| C. | 由A、B、C、D组成的两种盐的溶液反应可产生DB2气体 | |
| D. | 上述元素的非金属气态氢化物还原性最强的是E |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
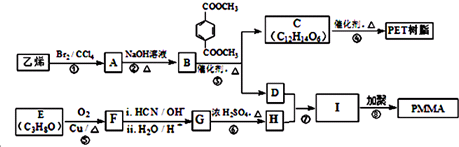
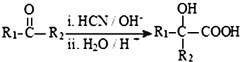 (R、R1、R2、R3均代表烃基)
(R、R1、R2、R3均代表烃基)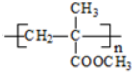 .
.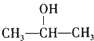 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2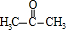 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | |
| B. | pH=8.3的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 0.1 mol AgCl和0.1 mol AgI混合后加入1 L水中,所得溶液中:c(Cl-)=c(I-) | |
| D. | 0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合后所得溶液中:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚有一定毒性,不能作消毒剂和防腐剂 | |
| B. | 纤维素可水解成葡萄糖,人类可从中获得生存所需的能量 | |
| C. | 2014年1月,国家首次将雾霾天气纳入自然灾情进行通报,雾霾是一种不同于胶体的分散系,它的形成与大量焚烧田间秸秆有关 | |
| D. | 煤经气化和液化两个物理变化过程,可变为清洁能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
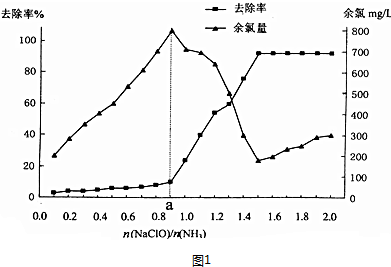
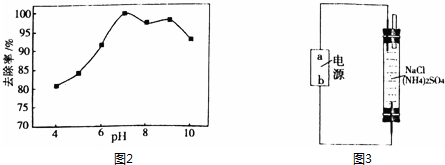
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com