
【题目】下列反应中,不属于加成反应的是( )
A.在一定条件下苯与液溴反应制取溴苯
B.苯与浓硝酸、浓硫酸混合共热制取硝基苯
C.在一定条件下,乙烯与氯化氢反应制取氯乙烷
D.苯在镍的催化作用下与氢气反应得到环己烷
科目:高中化学 来源: 题型:
【题目】下列关于用糯米制作米酒过程的叙述正确的是( )
A.发酵过程需要接种乳酸菌B.发酵过程需要保持空气流通
C.发酵过程需要控制好温度D.蒸熟糯米后马上加入酒曲
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关同分异构体数目的叙述中,正确的是
A. 苯乙烯和氢气完全加成的产物的一溴取代物有5种
B. 等物质的量的氯气与乙烷在光照条件下反应得到9种产物
C. 已知二氯苯有3种同分异构体,则四氯苯的同分异构体的数目为6种
D. 甲苯苯环上的一个氢原子被含4个碳原子的烷基取代,所得产物有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从石油中获取乙烯已成为目前生产乙烯的主要途径。请根据下图回答:

(1)以石油为原料,获取大量乙烯的主要方法是__________ (填字母代号)。
A 水解 B 裂解 C 分馏
(2)乙烯的结构简式是__________,B分子中官能团的名称是__________。
(3)A与B反应的化学方程式是_________,反应类型是__________,利用该反应制取乙酸乙酯的原子利用率为__________。(原子利用率=期望产物的总质量与生成物的总质量之比)
(4)某同学用图所示的实验装置制取少量乙酸乙酯。实验结束后,试管甲上层为透明且不溶于水的油状液体。

实验时,为分离出乙酸乙酯中混有的少量A和B,试管中应先加入__________,实验结束后,振荡试管甲,有无色气泡生成,其主要原因是__________ (用化学方程式表示),最后分离出乙酸乙酯用到的主要仪器是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醇酸树脂是一种成膜性好的树脂,下面是一种醇酸树脂的合成线路:

已知:
(1)有机物A中含有的官能团是____________(填汉字);写出B的结构简式是______________;E的分子式为_____________________。
(2)反应①的化学方程式是_________________,属于_______反应。
(3)反应①-④中属于取代反应的是________(填序号)。
(4)反应④的化学方程式为是_______________________。
(5)写出一种符合下列条件的与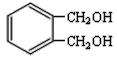 互为同分异构体的结构简式 ______________。
互为同分异构体的结构简式 ______________。
a.能与浓溴水反应生成白色沉淀,
b.通过核磁共振发现,苯环上只有两种不同化学环境的氢,且峰面积比为1∶1,
c.能发生消去反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用如图装置制取少量溴苯,并验证其中一种产物。试完成下列问题:

(1)在烧瓶a中装的试剂是___________、___________、_____________。
(2)导管b的作用有两个:
一是________________________________;
二是________________________________。
(3)导管c的下口可否浸没于液面中?为什么?
_______________________________________________________。
(4)反应过程中在导管c的下口附近可以观察到的现象是有______________出现,这是由于反应生成的________________遇水蒸气而形成的。
(5)反应完毕后,向锥形瓶d中滴加AgNO3溶液有____________________生成,反应的离子方程式:___________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对比饱和链烃、不饱和链烃的结构和性质,苯的独特性质具体来说是( )
A.难氧化,易加成,难取代
B.易取代,能加成,难氧化
C.易氧化,易加成,难取代
D.因是单双键交替结构,故易加成为环己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离常数(25℃) | Ka = 1.77×10 -4 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
①0.1 moI/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______c(HCO3 -)(填“>”、“<”或“=”)。
②常温下,pH相同的三种溶液
A.HCOONa B.NaCN C.Na2CO3,
其物质的量浓度由大到小的顺序是________(填编号)。
③已知25℃时,HCOOH( aq) +OH -( aq)=HCOO-(aq) +H2O(1) △H=-a kJ/mol
H+(aq) +OH-(aq) =H2O(1) △H=-b kJ/mol
甲酸电离的热化学方程式为__________________________________。
④将少量CO2通入NaCN溶液,反应的离子方程式是______________________。
⑤室温下,—定浓度的HCOONa溶液pH =9,用离子方程式表示溶液呈碱性的原因是:
______________________________,溶液中![]() =___________。
=___________。
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示。

①d点所示的溶液中离子浓度由大到小的顺序依次为_______________。
②b点所示的溶液中c(NH3·H2O)-c(NH4+)=_____(用溶液中的其它离子浓度表示)。
③pH =10的氨水与pH =4的NH4C1溶液中,由水电离出的c(H+)之比为____。
(3)已知Ksp(BaCO3) =2.6×l0-9,Ksp( BaSO4)=1.1×10-10.
①现将浓度为2×10-4mol/LNa2CO3溶液与BaCl2溶液等体积混合,则生成BaCO3沉淀所需BaCl2溶液的最小浓度为____mol/L。
②向含有BaSO4固体的溶液中滴加Na2CO3溶液,当有BaCO3沉淀生成时,溶液中![]() =___________(保留三位有效数字)。
=___________(保留三位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com