
A.M是铜,N是锌,R是硫酸溶液?
B.M是锌,N是铜,R是硫酸铜溶液?
C.M是银,N是锌,R是硝酸银溶液?
D.M是铁,N是铜,R是硝酸铜溶液?
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源:学习高手选修化学(反应原理人教版) 人教版 题型:021
|
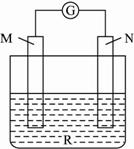
如图:电流计的指针会偏转,M极变粗,N极变细符合这种情况的是
| |
A. |
M是铜,N是锌,R是硫酸溶液 |
B. |
M是锌,N是铜,R是硫酸铜溶液 |
C. |
M是银,N是锌,R是硝酸银溶液 |
D. |
M是铁,N是铜,R是硝酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
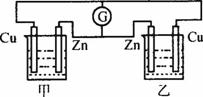
图1-2
A.电流计G的指针不动
B.甲、乙两装置都不是电解槽
C.甲装置中铜极上有气泡产生、乙装置中铜极上无气泡
D.乙装置中,H+离子浓度会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
如图:电流计的指针会偏转,M极变粗,N极变细符合这种情况的是( ) ?

A.M是铜,N是锌,R是硫酸溶液?
B.M是锌,N是铜,R是硫酸铜溶液?
C.M是银,N是锌,R是硝酸银溶液?
D.M是铁,N是铜,R是硝酸铜溶液?
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
(11分)某研究性学习小组为证明2Fe3+ + 2I- 2Fe2++ I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
按要求回答下列问题。
方案甲:
取5mL0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,再继续加入2mL CCl4,充分振荡。静置、分层,再取上层清液,滴加KSCN溶液。
(1)甲方案中能证明该反应为可逆反应的现象是 。
(2)有同学认为该方案设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是 。
方案乙:
取5mL0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,溶液呈棕黄色,再往溶液中滴加NH4F溶液,若看到 现象,即可证明该反应为可逆反应,请解释产生该现象的原因 。
方案丙:
设计如图原电池装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。
当指针读数变零后,在乙烧杯中加入1mol/L FeCl2溶液,若观察到灵敏电流计的指针向 方向偏转(填“左”、“右”或“不移动”),即可判断该反应为可逆反应,此时甲中石墨电极上的电极反应式为 。
【解析】(1)根据实验数据可知碘化钾是过量的,若反应是可逆反应,则溶液中一定存在铁离子,同时也必须生成单质碘。所以可以通过检验铁离子和单质碘来证明。
(2)因为碘离子和亚铁离子在空气中也可以被氧气氧化生成单质碘和铁离子,所以方案不是很严密。
(3)可以依据外界条件对平衡的影响来验证。因为Fe3+与F-络合生成无色的FeF63-,促使2Fe3+ +2I- 2Fe2+ + I2平衡朝逆反应方向移动,所以溶液颜色会变浅。
(4)在原电池中负极是失去电子的,碘离子失去电子,所以电子是从甲池流向乙池,所以电流计的指针向左偏转。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com