
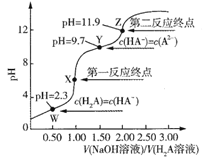
【题目】298K时,在0.10mol/LH2A溶液中滴入0.10mol/LNaOH溶液,滴定曲线如图所示。下列说法正确的是( )
A.该滴定过程应该选择石蕊作为指示剂
B.X点溶液中:c(H2A)+c(H+)=c(A2-)+2c(OH-)
C.Y点溶液中:3c(Na+)=2c(A2-)+2c(HA-)+2c(H2A)
D.0.01mol/LNa2A溶液的pH约为10.85
【答案】D
【解析】
滴定过程发生反应H2A+NaOH=H2O+NaHA、NaHA+NaOH=H2O+Na2A,第一反应终点溶质为NaHA,第二反应终点溶质为Na2A。
A.石蕊的的变色范围为5~8,两个反应终点不在变色范围内,所以不能选取石蕊作指示剂,故A错误;
B.X点为第一反应终点,溶液中的溶质为NaHA,溶液中存在质子守恒c(OH-)+ c(A2-)= c(H+)+ c(H2A),故B错误;
C.Y点溶液![]() =1.5,所以溶液中的溶质为等物质的量的NaHA和Na2A,根据物料守恒可知2c(Na+)=3c(A2-)+3c(HA-)+3c(H2A),故C错误;
=1.5,所以溶液中的溶质为等物质的量的NaHA和Na2A,根据物料守恒可知2c(Na+)=3c(A2-)+3c(HA-)+3c(H2A),故C错误;
D.Na2A溶液主要存在A2-的水解:A2-+H2O=HA-+OH-;据图可知当c(A2-)= c(HA-)时溶液pH=9.7,溶液中c(OH-)=10-4.3mol/L,而Na2A的第一步水解平衡常数Kh=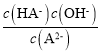 ,当c(A2-)= c(HA-)时Kh= c(OH-)=10-4.3,设0.01mol/LNa2A溶液中c(A2-)=amol/L,则c(OH-)amol/L,Kh=
,当c(A2-)= c(HA-)时Kh= c(OH-)=10-4.3,设0.01mol/LNa2A溶液中c(A2-)=amol/L,则c(OH-)amol/L,Kh=![]() ,解得a=10-3.15mol/L,即c(OH-)=10-3.15mol/L,所以溶液的pH=10.85,故D正确。
,解得a=10-3.15mol/L,即c(OH-)=10-3.15mol/L,所以溶液的pH=10.85,故D正确。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.有A、B、C三种无色溶液,它们分别是葡萄糖溶液、蔗糖溶液、淀粉溶液中的一种,甲同学做实验得出如下结论:
①A遇碘水变蓝色;②B能发生银镜反应。
(1)A是__,B是__,C是__。
(2)写出有关反应的化学方程式。
①蔗糖水解:_。
②淀粉水解:_。
Ⅱ.乙同学将蔗糖与淀粉的混合物放入水中,在一定条件下使其完全水解。
(3)“一定条件”指的是__。
(4)验证糖类发生水解的方法是__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NaOH溶液吸收烟气中的SO2,将所得的吸收液用三室膜电解技术处理,原理如图所示.下列说法错误的是
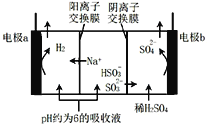
A.电极a为电解池阴极
B.阳极上有反应HSO3—-2e—+H2O=SO42—+3H+发生
C.当电路中通过1mol电子的电量时,理论上将产生0.5mol H2
D.处理后可得到较浓的H2SO4和NaHSO3产品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组利用传感器探究Na2CO3和NaHCO3的性质。
(查阅资料)
pH越小,c(OH-)越小,溶液碱性越弱。
(实验过程)
编号 | 实验操作 | 实验数据 |
实 验 Ⅰ | 测量下述实验过程的温度变化
|
|
实 验 Ⅱ | 测量下述实验过程的pH变化
|
|
(分析与解释)
(1)实验Ⅰ中,溶解时吸收热量的物质是_________。
(2)实验Ⅱ中,Na2CO3溶液和澄清石灰水反应的离子方程式为____,OH-未参与该反应的实验证据是_________。
(3)实验Ⅱ中,滴加NaHCO3溶液的pH变化与滴加Na2CO3溶液的有明显差异,原因是滴加NaHCO3溶液的烧杯中,参与反应的离子有____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上电化学法生产硫酸的工艺示意图如图,电池以固体金属氧化物作电解质,该电解质能传导O2-离子,已知S(g)在负极发生的反应为可逆反应,则下列说法正确的是( )
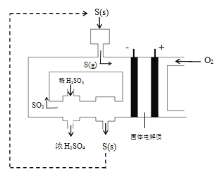
A.在负极S(g)只发生反应S-6e-+3O2-=SO3
B.该工艺用稀硫酸吸收SO3可提高S(g)的转化率
C.每生产1L浓度为98%,密度为1.84g/mL的浓硫酸,理论上将消耗30mol氧气
D.工艺中稀硫酸浓度增大的原因是水参与电极放电质量减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据公安部2019年12月统计,2019年全国机动车保有量已达3.5亿。汽车尾气排放的碳氢化合物、氮氧化物及碳氧化物是许多城市大气污染的主要污染物。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知:C(s)+O2(g)=CO2(g) △H1=393.5kJ·mol1
2C(s)+O2(g)=2CO(g) △H2=221.0kJ·mol1
N2(g)+O2(g)=2NO(g) △H3=+180.5kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式___。
(2)对于2NO(g)+2CO(g)![]() N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
下列能说明该反应已经达到平衡状态的是___(填字母代号)。
A.![]() 比值不变
比值不变
B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆
D.容器中混合气体的平均摩尔质量不变
(3)使用间接电化学法可处理燃煤烟气中的NO,装置如图2所示。
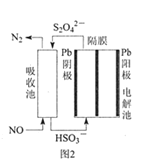
已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式__。用离子方程式表示吸收池中除去NO的原理___。
(4)T1温度时在容积为2L的恒容密闭容器中发生反应:2CO(g)+O2(g)![]() 2CO2(g) △H<0。实验测得:v正=v(CO)消耗=2v(O2)消耗=k正c2(CO)·c(O2),v逆=(CO2)消耗=k逆c2(CO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(CO)、n(O2)如表:
2CO2(g) △H<0。实验测得:v正=v(CO)消耗=2v(O2)消耗=k正c2(CO)·c(O2),v逆=(CO2)消耗=k逆c2(CO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(CO)、n(O2)如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(CO)/mol | 2 | 1.2 | 0.8 | 0.4 | 0.4 | 0.4 |
n(O2)/mol | 1.2 | 0.8 | 0.6 | 0.4 | 0.4 | 0.4 |
①T1温度时![]() =___L/mol。
=___L/mol。
②若将容器的温度改变为T2时其k正=k逆,则T2__T1(填“>”、“<”或“=")。
II.“低碳经济”备受关注,CO2的有效开发利用成为科学家研究的重要课题。在0.1MPa、Ru/TiO2催化下,将一定量的H2和CO2置于恒容密闭容器中发生反应X:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
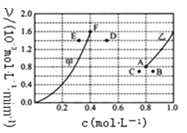
(5)为探究反应X的反应速率与浓度的关系,向恒容密闭容器中通入浓度均为1.0molL-1的H2与CO2。恒温条件下,根据相关数据绘制出反应速率与浓度关系曲线:v正~c(CO2)和v逆~c(H2O)。则与曲线v正~c(CO2)相对应的是如图___曲线。(填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线乙对应的平衡点可能为___(填字母)。
(6)温度为T时,向10L密闭容器中充入5molH2和CO2的混合气体,此时容器内压强为5P,两种气体的平衡转化率ɑ与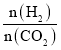 的关系如图所示:
的关系如图所示:
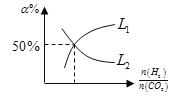
①图中CO2的平衡转化率可用表示___(L1或L2)
②该温度下,反应X的平衡常数Kp=___。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图像分别表示有关反应的反应过程与能量变化的关系。据此判断下列说法正确的是
A. 石墨转变为金刚石的反应是吸热反应
B. 白磷比红磷稳定
C. S(g)=S(s) ΔH>0
D. H2(g)+I2(g)![]() 2HI(g) ΔH>0
2HI(g) ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种物质直接的转化如图所示,其中不能一步实现的是( )
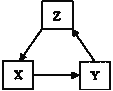
A | B | C | D | |
X | C | NaOH | CH3CH2OH | N2 |
Y | CO | Na2CO3 | CH3CHO | NH3 |
Z | CO2 | NaHCO3 | CH3COOH | NO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计了由乙醇合成乙二醇的路线如下。下列说法正确的是

A. X可以发生加成反应
B. 步骤①的反应类型是水解反应
C. 步骤②需要在氢氧化钠醇溶液中反应
D. 等物质的量的乙醇、X完全燃烧,消耗氧气的量不相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com