
Q、W、X、Y、Z是原子序数依次增大的短周期主族元素,Q、Y在周期表中相对位置如下:
Q |
|
|
|
|
|
| Y |
|
|
已知:Q元素最低负化合价的绝对值与其原子最外层电子数相等,W、Y同主族,X是地壳中含量最多的金属元素。下列说法正确的是
A.Q的最高价氧化物属于离子化合物
B.W和氢元素组成的化合物分子中只含有极性共价键
C.Q、X、Y、Z元素最高价氧化物对应的水化物中酸性最强的是HZO4
D.工业上可用电解熔融的X的氯化物方法来制备X单质
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源:2015-2016学年山东省临沂市河东区高一上期末化学试卷(解析版) 题型:填空题
(1)CO2的摩尔质量为 ;88 g CO2的物质的量为 ,在标准状况下的体积约为 。
(2)1.5 molH3PO 4的质量是 ,含有 个H3PO 4分子。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高二下期末化学试卷(解析版) 题型:推断题
实验室用燃烧法测定某种α- 氨基酸X (CxHyOzNp)的分子组成。取3.34 g X放在纯氧中充分燃烧,生成CO2、H2O和N2。现用下图所示装置进行实验(铁架台、铁夹、酒精灯等未画出),请回答有关问题:
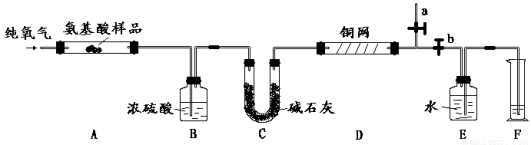
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通一段时间的纯氧气,这样做的目的是 ;之后则需关闭止水夹a,打开止水夹b。
(2)上述装置中A、D处都需要用酒精灯加热,操作时应先点燃 处的酒精灯。
(3)装置D的作用是 。
(4)实验结果:
①B中浓硫酸增重1.62 g,C中碱石灰增重7.04 g,F中收集到224 mL气体(标准状况)。
②X的相对分子质量为167,它是通过 测定的(填一种现代化学仪器)
试通过计算确定该有机物X的分子式(写出计算过程)。
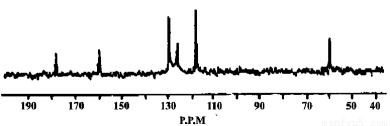
(5)另取3.34 g X与0.2 mol/L 的NaOH溶液反应,最多能中和NaOH溶液200 mL,有机物X的13C-NMR(即核磁共振碳谱,其作用与核磁共振氢谱类似)如下图所示。试确定有机物X的结构简式为 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省济宁市高二下期末化学试卷(解析版) 题型:选择题
可以证明可逆反应N2+3H2?2NH3已达到平衡状态的是
①一个N≡N键断裂的同时,有6个N﹣H键断裂
②v(N2)=0.2mol•L-1•min-1,v(NH3)=0.4mol•L﹣1•min-1
③保持其他条件不变时,体系压强不再改变;
④恒温恒容时,混合气体的密度保持不变;
⑤NH3、N2、H2的体积分数都不再改变。
A. ①②④ B. ①③⑤ C. ②③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省抚顺市协作校高一下期末化学试卷(解析版) 题型:填空题
下表是元素周期表的一部分(短周期),针对表中用字母标出的元素,除特别说明外,按要求用化学用语回答下列问题:

(1)在这些元素中,化学性质最不活泼的是 (填具体元素符号),其原子结构示意图为 。
(2)表中K代表的元素名称为 ,其在周期表中的位置为 。
(3)某元素原子M层电子数是第一层电子数的2倍,另一元素原子最外层电子数是次外层电子数的3倍,二者形成的化合物的化学式是 。
(4)最高价氧化物的水化物中碱性最强的化合物的电子式是 。
(5)GA3和HA3中沸点较高的是 (填具体化学式),GA3的水溶液呈 性,D的简单阳离子和该水溶液反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省抚顺市协作校高一下期末化学试卷(解析版) 题型:选择题
在一定温度下,密闭容器内某一反应中M、N两种气体的物质的量随反应时间的变化曲线如图,下列表述中正确的是
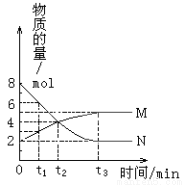
A.反应的化学方程式为:N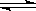 2M
2M
B.t2时,正逆反应速率相等,达到平衡
C.t3时,保持恒温恒容,再充入N,N的转化率保持不变
D.t3时,其他条件不变,改变温度,平衡一定发生移动
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省抚顺市协作校高一下期末化学试卷(解析版) 题型:选择题
下列叙述正确的是
A. 18OD-离子中,质子数、电子数、中子数之比为9∶10∶11
B. H2O和CCl4分子中所有原子均满足最外层8电子结构
C. 元素性质呈周期性变化的实质是元素化合价呈周期性变化
D. 115号元素位于周期表第六周期第ⅤA族
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁省大连市高一下期末化学试卷(解析版) 题型:选择题
下列四个数据是在不同条件下测出的合成氨反应的速率,其中最快的是( )
A.V(H2)= 0.1 mol /(L · min)
B.V(N2)= 0.1mol /(L · min)
C.V(NH3)= 0.15mol /(L · min)
D.V(N2)= 0.002mol /(L · s)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年新疆伊犁州伊宁二中高二下期末化学试卷(解析版) 题型:填空题
(12分) 东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_ _,提供孤电子对的成键原子是__ ___。
③氨的沸点_____(“高于”或“低于”)膦(PH3),原因是____ ;氨是____ _分子(填“极性”或“非极性”),中心原子的轨道杂化类型为____。
(3)单质铜及镍都是由______键形成的晶体:元素同与镍的第二电离能分别为:I(Cu)=1959kJ/mol,I(Ni)=1753kJ/mol,I(Cu)>I(Ni)的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。
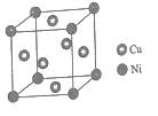
晶胞中铜原子与镍原子的数量比为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com