
科目:高中化学 来源: 题型:
 图中,P为可自由滑动的活塞,关闭K,V(A)=aL,V(B)=0.8aL(连通管的体积忽略不计).在相同温度和有催化剂存在的条件下,分别向容器A、B中各充入1molN2和3molH2,发生反应N2(g)+3H2(g)
图中,P为可自由滑动的活塞,关闭K,V(A)=aL,V(B)=0.8aL(连通管的体积忽略不计).在相同温度和有催化剂存在的条件下,分别向容器A、B中各充入1molN2和3molH2,发生反应N2(g)+3H2(g)  2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.
2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省扶沟县高级中学高二第三次考试化学试卷(带解析) 题型:填空题
(12分)“生物质"是指由植物或动物生命体衍生得到的物质的总称。“生物质能”是人类解决能源危机的一种重要的能源。“生物质”在一定条件下可气化为CO、H2等原料气,进而合成甲醇和二甲醚(CH3OCH3),相关反应为: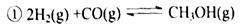

请根据图示回答问题: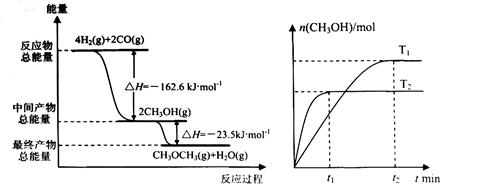
(1) 由H2和CO合成二甲醚的热化学方程式是 。
(2) 在T1、T2温度下,向两个容积相同的密闭容器中分别通入1molCO和2molH2合成甲醇,则T1、T2温度下对应反应的平衡常数K1_______K2(选填“<”、“>”或“=”)。
(3) 在一定条件下,向一个容积可变的密闭容器中充入4molH2、2molCO、1molCH3OCH3(g)和1molH20(g),经一定时间反应②达到平衡状态,此时测得混合气体密度是相同条件下起始时的1.6倍。反应开始时正、逆反应速率的大小关系为V(正)_______V(逆)(选填“ >”、“< ”或“=”),平衡时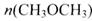 =_________mol。
=_________mol。
(4) 右图为绿色电源“二甲醚燃料电池”的工作原理示意图。(a、b均为多孔性Pt电极)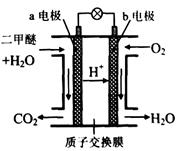
b电极是_______极:(填“正”或“负”)
a电极上的电极反应为___ ____。
查看答案和解析>>
科目:高中化学 来源:2014届河南省高二第三次考试化学试卷(解析版) 题型:填空题
(12分)“生物质"是指由植物或动物生命体衍生得到的物质的总称。“生物质能”是人类解决能源危机的一种重要的能源。“生物质”在一定条件下可气化为CO、H2等原料气,进而合成甲醇和二甲醚(CH3OCH3),相关反应为:


请根据图示回答问题:

(1) 由H2和CO合成二甲醚的热化学方程式是 。
(2) 在T1、T2温度下,向两个容积相同的密闭容器中分别通入1molCO和2molH2合成甲醇,则T1、T2温度下对应反应的平衡常数K1_______K2(选填“<”、“>”或“=”)。
(3) 在一定条件下,向一个容积可变的密闭容器中充入4molH2、2molCO、1molCH3OCH3(g)和1molH20(g),经一定时间反应②达到平衡状态,此时测得混合气体密度是相同条件下起始时的1.6倍。反应开始时正、逆反应速率的大小关系为V(正)_______V(逆)(选填“ >”、“< ”或“=”),平衡时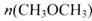 =_________mol。
=_________mol。
(4) 右图为绿色电源“二甲醚燃料电池”的工作原理示意图。(a、b均为多孔性Pt电极)
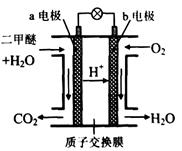
b电极是_______极:(填“正”或“负”)
a电极上的电极反应为___ ____。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年湖北省荆门市夷陵中学、钟祥一中高三(上)第二次联考化学试卷(解析版) 题型:填空题
 2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.
2NH3(g);△H=-92.4kJ/mol.达到平衡后,V(B)=0.6aL.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com