
【题目】(1)互为同分异构体的四种有机物A、B、C、D,它们的相对分子质量为74,完全燃烧只生成CO2和H2O,经分析其含氧元素的质量分数为43.3%,则这些有机物的分子式为___________,
(2)已知A、B、C、D分子结构中均含甲基,把它们分别进行下列实验以鉴别之,其实验记录如下:
| NaOH溶液 | 银氨溶液 | 新制Cu(OH)2 | 金属钠 |
A | 中和反应 | —— | 溶 解 | 产生氢气 |
B | —— | 有银镜 | 加热后有红色沉淀 | 产生氢气 |
C | 水解反应 | 有银镜 | 加热后有红色沉淀 | —— |
D | 水解反应 | —— | —— | —— |
则A、B、C、D的结构简式分别为
A____________ B____________ C____________ D____________。
【答案】 C3H6O2 CH3CH2COOH CH3CH(OH)CHO HCOOCH2CH3 CH3COOCH3
【解析】(1)互为同分异构体的四种有机物A、B、C、D,它们的相对分子质量为74,完全燃烧只生成CO2和H2O,经分析其含氧元素的质量分数为43.3%,则含有的氧原子个数是![]() ,则碳氢的总相对分子质量是74-32=42,42÷14=3,所以这些有机物的分子式为C3H6O2;(2)A能发生中和反应,则A中含有羧基,不能和银氨溶液反应,则不含醛基,和钠反应生成氢气,能溶解氢氧化铜,说明含有羧基,且含甲基,则符合条件的A是丙酸,其结构简式为CH3CH2COOH;B不和碱反应,说明不含羧基,能发生银镜反应说明含有醛基,能和钠反应生成氢气,则含有醇羟基,且含甲基,则符合条件的B是2-羟基丙醛,其结构简式为CH3CHOHCHO;C能发生水解反应说明含有酯基,能发生银镜反应说明含有醛基,不能和钠反应说明不含醇羟基或羧基,且含甲基,则符合条件的C是甲酸乙酯,其结构简式为HCOOCH2CH3;D能发生水解反应说明含有酯基,不能发生银镜反应说明不含醛基,不和钠反应说明不含醇羟基或羧基,且含甲基,则符合条件的D是乙酸甲酯,其结构简式为CH3COOCH3。
,则碳氢的总相对分子质量是74-32=42,42÷14=3,所以这些有机物的分子式为C3H6O2;(2)A能发生中和反应,则A中含有羧基,不能和银氨溶液反应,则不含醛基,和钠反应生成氢气,能溶解氢氧化铜,说明含有羧基,且含甲基,则符合条件的A是丙酸,其结构简式为CH3CH2COOH;B不和碱反应,说明不含羧基,能发生银镜反应说明含有醛基,能和钠反应生成氢气,则含有醇羟基,且含甲基,则符合条件的B是2-羟基丙醛,其结构简式为CH3CHOHCHO;C能发生水解反应说明含有酯基,能发生银镜反应说明含有醛基,不能和钠反应说明不含醇羟基或羧基,且含甲基,则符合条件的C是甲酸乙酯,其结构简式为HCOOCH2CH3;D能发生水解反应说明含有酯基,不能发生银镜反应说明不含醛基,不和钠反应说明不含醇羟基或羧基,且含甲基,则符合条件的D是乙酸甲酯,其结构简式为CH3COOCH3。


科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. CH3CH=CHCH3,分子中的四个碳原子在同一直线上
B. 乙醛能使溴水出现褪色觋象,是因为乙醛发生了氧化反应
C. 在酸性条件下,CH3CO18OCH2CH3的水解产物是CH3CO18OH和CH3CH2OH
D. 聚合物(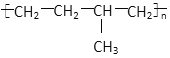 )可由单体CH3CH=CH2和CH2=CH2加聚制得
)可由单体CH3CH=CH2和CH2=CH2加聚制得
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是利用一种微生物将废水中的有机物(假设是淀粉)的化学能直接转化为电能,并利用此电能在铁上镀铜,下列说法中正确的是
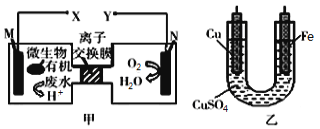
A.质子透过离子交换膜由右向左移动
B.铜电极应与X相连接
C.M电极反应式:(C6H10O5)n+7nH2O-24ne-=6nCO2↑+24nH+
D.当N电极消耗0.25mol气体时,则铁电极增重16g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1)A2B的电子式__________;A2B2的电子式__________。
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积1L,假设变化前后溶液体积变化忽略不计)组装成原电池(如右图所示)。在b电极上发生的反应可表示为:PbO2+4H++SO42-+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为__________。

(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中,溶液由黄色逐渐变为浅绿色,该反应的离子方程式为________________________________________。
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池(右图),则在该原电池工作时,石墨一极发生的反应可以表示为______________________________。石墨除形成原电池的闭合回路外,所起的作用还有:________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于原电池的叙述正确的是
A. 构成原电池的正极和负极必须是两种不同的金属
B. 原电池是将化学能转变为电能的装置
C. 原电池中电子流出的一极是负极,该极被还原
D. 原电池工作时,电流的方向是从负极到正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组混合物总物质的量均为a mol,当每组物质以任意物质的量之比混合完全燃烧时,消耗O2的量不变的是
A. 甲烷、甲醇 B. 乙烯、环丙烷
C. 乙炔、苯 D. 乙醇、丙烯酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《天工开物》第七卷《陶埏(陶瓷)》中记载“水火既济而土合……后世方土效灵,人工表异,陶成雅器,有素肌、玉骨之象焉”,以上所述的“陶成雅器”的主要原料是
A. 黏土 B. 纯碱、石灰石、石英砂
C. 黏土、石灰石 D. 二氧化硅、硅酸钙、硅酸铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G都是链状有机物,它们的转化关系如图所示,D的相对分子质量与E相差42,请回答下列问题;
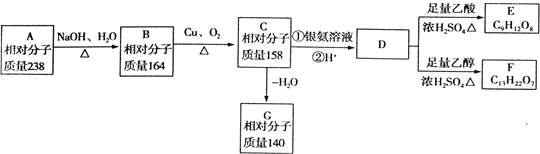
(1)D中含有的官能团是_________,各种官能团的个数比是________。
(2)D的核磁共振氢谱图上有3个峰,且峰面积之比为1:3:6,请写出D的结构简式__________。
(3)写出B生成C的化学方程式______________________________________.
(4)A只含一种官能团,则A的结构简式为___________。
(5)芳香族化合物H与G互为同分异构体,1molH与足量的钠反应产生1.5molH2,与足量的氢氧化钠溶液反应消耗2molNaOH,且H苯环上的一氯代物只有两种,写出符合条件的H的结构简式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气在工业合成中广范应用。
(1)通过下列反应可以制备甲醇:
CO(g)+2H2(g)![]() CH3OH(g) ΔH=-90.8kJ/mol,
CH3OH(g) ΔH=-90.8kJ/mol,
CO2(g)+H2(g)![]() CO(g)+H2O(g) ΔH=+41.3kJ/mol
CO(g)+H2O(g) ΔH=+41.3kJ/mol
请写出由CO2和H2制取甲醇的热化学方程式______________。
(2)己知合成氨的反应为:N2+3H2![]() 2NH3 △H<0。某温度度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和怛容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请冋答下列问题:
2NH3 △H<0。某温度度下,若将1molN2和2.8molH2分别投入到初始体积为2L的恒温恒容、恒温恒压和怛容绝热的三个密闭容器中,测得反应过程中三个容器(用a、b、c表示)内N2的转化率随时间的变化如图所示,请冋答下列问题:

①图中代表反应在恒容绝热容器中进行的曲线是________(用a、b、c表示)。
②曲线a条件下该反应的平衡常数K=_____________。
③b容器中M点,v(正)________v(逆)(填“大于”、“小于”或“等于”)。
(3)利用氨气可以设计成高能环保燃料电池,用该电池电解含有NO2-的碱性工业废水,在阴极产生N2。阴极电极反应式为________;标准状况下,当阴极收集到11.2LN2时,理论上消耗NH3的体积为_____________。
(4)常温下,用氨水吸收CO2可得到NH4HCO3溶液,在NH4HCO3溶液中c(NH4+)____ c(HCO3-) (填“>”、“<”或“=”);反应NH4++HCO3-+H2O![]() NH3H2O+H2CO3的平衡常数K=_______。
NH3H2O+H2CO3的平衡常数K=_______。
(已知常温下NH3H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7, K2=4×10-11)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com