
下列制备溶胶的方法可行的是( )
①0.5mol·L-1BaCl2溶液和等体积2mol·L-1H2SO4溶液混合并振荡 ②把1mL饱和的FeCl3溶液逐滴加入20mL的沸水中,边加边振荡 ③把1mLNa2SiO3溶液加入10mL1mol·L-1HCl溶液中用力振荡
A.只有①② B.只有①③ C.只有②③ D.都可行
科目:高中化学 来源: 题型:阅读理解

| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 实验序号 | 实验步骤 | 实验现象 | 结论 |
| ① | 用激光笔照射甲组制得的PAC溶液 | 光亮的通路 | |
| ② | 取乙组制得的样品少许加入铝试剂阿罗明拿 | 变成玫瑰红色 | |
| ③ | 取丙组样品少许,溶于适量的水制得的淡黄色透明液体中加入氟化铵 |
查看答案和解析>>
科目:高中化学 来源:江苏省盐城市2010届高三第二次调研考试化学试题 题型:022
聚合氯化铝(PAC)可以看成是AlCl3水解成为Al(OH)3的中间产物,其化学通式为[Al2(OH)nCl6-n]m(m≤10,n=3~5).若式中,n接近于6或等于6,则可称为铝溶胶.聚合氯化铝是一种无机高分子混凝剂.某合作学习小组的同学在查阅文献资料后拟用不同的方法制备聚合氯化铝.
(1)甲组用凝胶-溶胶法,它们用结晶氢氧化铝、烧碱、CO2及盐酸为试剂生产,其中涉及的氢氧化铝与烧碱反应的化学方程式为:________.
(2)乙组采用不足量酸溶法,原料主要是铝加工的下脚料铝屑、铝灰和铝渣等,反应原理为:2Al+(6-n)HCl+nH2O=Al2(OH)nCl6-n+3H2↑.该制备方法工艺简单、成本低,利用本身是放热反应,故不需要加热,可能缺点有:________(列举一条).
(3)丙组拟用高岭土(Al2O3·2SiO2·2H2O)等为原料,经焙烧、盐酸浸取、聚合、熟化、蒸发、干燥等步骤得到固体PAC.其中液体PAC蒸发时,适宜在110℃左右,你认为适宜的加热方法是________.
(4)丁组同学对甲、乙、丙组同学制得的样品进行定性实验,请你补充下列实验报告

(5)戊组同学对丙组固体样品请质检部门用27Al-NMR测试,其中的分散质主要是:Al13O4(OH)24Cl7,属于优质产品.他们另取样品m g少许放在坩埚中充分加热并灼烧,最终得到的固体产物为:________,若得到固体n g,则制得的样品中铝的质量分数为________.
查看答案和解析>>
科目:高中化学 来源:2014届江西省抚州市高二下学期期末考试化学试卷(解析版) 题型:填空题
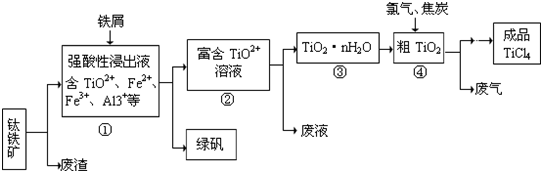
四氯化钛(TiCl4)是制取航天航空工业材料——钛合金的重要原料。由钛铁矿(主要成为是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:

回答下列问题:
往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性。该过程中有如下反应发生:
2Fe3++Fe=3Fe2+
2TiO2+(无色)+Fe+4H+=2Ti3+(紫色) +Fe2++2H2O
Ti3+(紫色)+Fe3++H2O=TiO2+(无色)+Fe2++2H+
加入铁屑的作用是 。
(2)在②→③工艺过程中需要控制条件以形成TiO2·nH2O溶胶,该溶胶的分散质颗粒直径大小在 范围。
(3)若把③中制得的固体TiO2·nH2O用酸清洗除去其中的Fe(OH)3杂质,还可以制得钛白粉。已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+ Fe3++3H2O的平衡常数K=
。
Fe3++3H2O的平衡常数K=
。
(4)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出④中TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式: 。
(5)上述工艺具有成本低、可用低品位矿物为原料等优点。依据绿色化学理念,该工艺流程中存在的不足之处是 (只要求写出一项)。
(6)依据下表信息,要精制含少量SiCl4杂质的TiCl4的,可采用 方法。
|
|
TiCl4 |
SiCl4 |
|
熔点/℃ |
-25.0 |
-68.8 |
|
沸点/℃ |
136.4 |
57.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com