
分析 (1)依据离子方程式的电荷守恒和原子守恒书写判断产物;
(2)还原剂是元素化合价反应后升高,结合化合价变化分析判断;
(3)依据四个反应分析判断产物.
解答 解:(1)依据离子方程式的电荷守恒和原子守恒书写判断产物;反应①中为4SO42-,②反应中为2H2O,
故答案为:4SO42-,2H2O;
(2)还原剂是元素化合价反应后升高,反应③中硫元素化合价从-1价变化为0价,所以反应中的还原剂是FeS2;反应④中氧气得电子被还原生成的为还原产物SO42-;
故答案为:FeS2;SO42-;
(3)依据①②③④的离子方程式,分析判断最终的生成物为硫酸亚铁和硫酸,
故答案为:FeSO4 H2SO4.
点评 本题考查了氧化还原反应的电荷守恒、原子守恒的应用,氧化还原反应概念的分析判断,掌握特征变化、分析反应实质,判断概念的由来.


科目:高中化学 来源: 题型:选择题
| A. | (CH3)2CHCl | B. | CH3C(CH3)2I | C. | (CH3)3COOCCH2CH3 | D. | CH3C(CH3)2CH2Br |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新戊烷 C(CH3)4 | B. | 3-乙基-1-丁烯 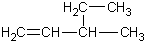 | ||
| C. | 2-甲基-2,4-己二烯 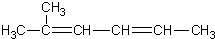 | D. | 2,2,3-三甲基戊烷 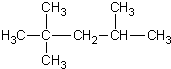 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | E(3s)>E(3p)>E(3d) | B. | E(3s)>E(2s)>E(2 p) | C. | E(4f)>E(3d)>E(4s) | D. | E(5s)>E(4s)>E(4f) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 某模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )
某模拟“人工树叶”电化学实验装置如下图所示,该装置能将H2O和CO2转化为O2和燃料(C3H8O),下列说法正确的是( )| A. | 该装置将化学能转化为光能和电能 | |
| B. | a电极的反应为:3CO2+18H+-18e-═C3H8O+5H2O | |
| C. | 每生成1 mol O2,有44 g CO2被还原 | |
| D. | 该装置工作时H+从b极区向a极区迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在基态多电子原子中,p轨道电子能量不一定高于s轨道电子能量 | |
| B. | 核外电子排布由1s22s22p63s1→1s22s22p6 的变化需要吸收能量 | |
| C. | 某元素基态原子的电子排布图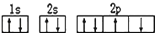 | |
| D. | Ca2+离子基态电子排布式为1s22s22p63s23p6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,0.1molC3H8所含有的共价键数目为1.1 NA | |
| B. | 1mol苯分子中,含有碳碳双键的数目为3 NA | |
| C. | 常温常压下,15g甲基(-CH3)所含的电子数为10NA | |
| D. | 现有乙烯、丙烯的混合气体共14 g,其原子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 分子式为C2H4O2的有机化合物性质相同 | |
| B. | 由如图可得H2O2分解的热化学方程式为2H2O2(aq)═2H2O(l)+O2(g),△H=(E1-E2)kJ•mol-1 | |
| C. | Al2O3具有很高的熔点,可用于制造熔融烧碱的坩埚 | |
| D. | Na2O2与CO2反应产生1 mol O2理论上转移的电子数约为26.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇的分子式:CH3CH2OH | B. | CH3COCH3的官能团名称:醚键 | ||
| C. | 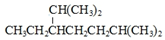 的名称为:2,6-二甲基-3-乙基庚烷 的名称为:2,6-二甲基-3-乙基庚烷 | D. | 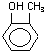 的类别:醇类 的类别:醇类 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com