
【题目】常温下10mL浓度均为0.1mol·L-1的HX和HY两种一元酸溶液加水稀释过程中的pH随溶液体积变化曲线如图所示。则下列说法不正确的是

A. 电离常教:K(HX)<K(HY)
B. 浓度均为0.1mol·L-1的HX和HY的混合溶液中:c(X-)+c(HX)=c(Y-)+ c(HY)
C. 浓度均为0.1mol·L-1的NaX和NaY的混合溶液中:c(Na+)>c(Y-)>c(X-)>c(OH-)>c(H+)
D. a点水的电离度大于b点水的电离度
【答案】D
【解析】A.浓度均为0.1mol/L的HX和HY两种一元酸,HY溶液的pH=2,HX的pH>2,说明HY溶液中氢离子浓度大于HX,则HY的酸性比HX强,所以HX的电离常数K(HX)小于HY的电离常数K(HY),A正确;B.根据物料守恒可知浓度均为0.1mol·L-1的HX和HY的混合溶液中:c(X-)+c(HX)=c(Y-)+ c(HY),B正确;C.HY的酸性比HX强,则NaX的水解程度大,所以溶液中c(Y-)>c(X-),则溶液中离子浓度大小关系:c(Na+)>c(Y-)>c(X-)>c(OH-)>c(H+),C正确;D.a、b两点溶液中氢离子浓度相同,对水的电离的抑制程度相同,所以a点水的电离程度等于b点水的电离程度,D错误;答案选D。


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、W、Q的原子序数依次增。X、Y是非金属元素X、Y、Q元素的原子最高能级上电子数相等;Z元素原子的最外层电子数是次外层的两倍;W元素原子核外有三种不同的能级且原子中p亚层与s亚层电子总数相等;Q元素电离能分别是I1=496,I2=4562,I3=6912。回答下列问题:
(1)基态Q原子的核外电子排布式是____________________。
(2)Q、W形成的化合物Q2W2中的化学键类型是______________。
(3)Y能与氟元素形成YF3,该分子的空间构型是_______,该分子属于______分子(填“极性”或“非极性”)。Y与X可形成具有立体结构的化合物Y2X6,该结构中Y采用______杂化。
(4)Y(OH)3是一元弱酸,其中Y原子因缺电子而易形成配位键,写出Y(OH)3在水溶液中的电离方程式_______________。
(5) Z的一种单质晶胞结构如下图所示。
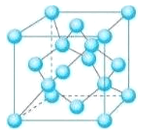
①该单质的晶体类型为___________。
②含1 mol Z原子的该晶体中共有_____mol化学键。
③己知Z的相对原子质量为M,原子半径为r pm,阿伏伽德罗常数的值为NA,则该晶体的密度为____g·cm-3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:维生素A、维生素C、碘元素、铁元素、淀粉、油脂。请选择正确答案填在相应的空格里。
①人体缺乏某种维生素会引起坏血病,这种维生素是__________。
②人体缺乏某种微量元素会发生贫血,这种微量元素是__________。
③既能为人体提供热量,又能提供必需脂肪酸的物质是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体酸燃料电池以CsHSO4固体为电解质传递H+,其基本结构见下图。下列有关说法错误的是

A. a极为负极,电极上发生氧化反应
B. 电池总反应可表示为:2H2+O2=2H2O
C. 外电路中电子由b电极通过导线流向a电极
D. 该装置工作时把电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于物质的用途的说法不正确的是( )
A. SO2可用于漂白纸浆 B. 氢氧化铝、碳酸氢钠可用于治疗胃酸过多
C. 钢罐可用于储运浓硫酸 D. 磁性氧化铁可用于制备红色颜料和油漆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是

A. d的氢化物比b的氢化物稳定
B. d与c不能形成化合物
C. a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a
D. 原子半径的大小顺序是a>b>c>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三室式电渗析法处理含Na2SO4废水的原理如图所示,采用惰性电极,ab、cd均为离子交换膜,在直流电场的作用下,两膜中间的Na+和SO42-可通过离子交换膜,而两端隔室中离子被阻挡不能进入中间隔室。下列叙述正确的是

A. 通电后中间隔室的SO42-离子向正极迁移,正极区溶液pH增大
B. 该法在处理含Na2SO4废水时可以得到NaOH和H2SO4产品
C. 负极反应为2H2O 4e– = O2+4H+,负极区溶液pH降低
D. 当电路中通过1mol电子的电量时,会有0.5mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。

下列分析不正确的是
A.①代表滴加H2SO4溶液的变化曲线
B.b点,溶液中大量存在的离子是Na+、OH–
C.c点,两溶液中含有相同量的OH–
D.a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池与现代人的生活密切相关,某同学为了研究原电池原理设计了如图所示的装置。下列说法错误的是

A. X、Y不用导线连接时,铜棒上会有银析出
B. X和Y用导线连接时,银棒上发生的电极反应为Ag++e-==Ag
C. X和Y用导线连接时,电子由银经导线移向铜,再经电解质溶液移向银
D. 无论X和Y是否用导线连接,铜棒均会溶解,溶液都从无色逐渐变成蓝色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com