
金刚烷是一种重要的化工原料,工业上可通过下列途径制备:

请回答下列问题:
44.环戊二烯分子中最多有________个原子共平面;
45.金刚烷的分子式为________,其分子中的—CH2—基团有________个;
46.下面是以环戊烷为原料制备环戊二烯的合成路线:
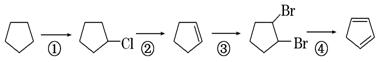
其中,反应①的产物名称是_________________________________________,
反应②的反应试剂和反应条件是________________,反应③的反应类型是________________;
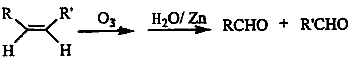 47.已知烯烃能发生如下反应:
47.已知烯烃能发生如下反应:
请写出下列反应产物的结构简式:
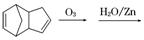 ____________________________________________;
____________________________________________;
48.A是二聚环戊二烯的同分异构体,能使溴的四氯化碳溶液褪色,A经高锰酸钾酸性溶液加热氧化可以得到对苯二甲酸[提示:苯环上的烷基(—CH3,—CH2R,—CHR2)或烯基侧链经高锰酸钾酸性溶液氧化得羧基],写出A所有可能的结构简式(不考虑立体异构)。
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
已知:(A)Cu2+,Fe2+在pH为4~5的条件下不水解而Fe3+却几乎全部水解;(B)双氧水(H2O2)是强氧化剂,在酸性条件下,它的还原产物是H2O。用粗氧化铜(CuO中含少量Fe)制取CuCl2溶液过程如下:
①取50mL的盐酸,加入一定量的粗CuO加热搅拌,充分反应后过滤,溶液的pH是3
②向滤液中加入双氧水,搅拌。
③向②中加入过量纯CuO,微热,搅拌,此时测定溶液的pH为4,过滤。
④把③所得滤液浓缩。
(1)②中发生反应的离子方程式是 。
(2)③中过滤后滤渣的成分是 。
(3)①③中如何用pH试纸测定溶液的pH值: 。
(4)③中pH升高的原因是: 。(用离子方程式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值。下列叙述正确的是( )
A.1mol甲苯含有6NA个C-H键
B.25℃,pH =13的NaOH溶液中含有OH-的数目为 0.1NA
C.标准状态下,33.6L氟化氢中含有氟原子的数目为1.5NA
D. 丙烯和环丙烷组成的42 g混合气体中氢原子的个数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
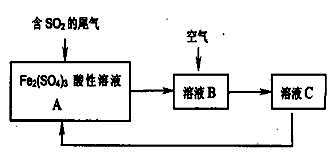
如图是一种综合处理SO2废气的工艺流程。若每步反应都完全,下列说法正确的是
(设反应过程中溶液的体积不变)( )
A.溶液B中发生的反应为:2SO2+O2→2SO3
B.由反应过程可推知氧化性:O2>Fe3+>SO42-
C.溶液的pH:A>B>C
D.A与C溶液成分相同,但浓度之比不同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol·L-1的盐酸与等体积水混合后pH=1
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
温度t℃时,某NaOH稀溶液中[H+]=10-a mol·L-1,[OH-]=10-b mol·L-1,已知a+b=12,请回答下列问题:
(1)该温度下水的离子积常数KW=
________________________________________________________________________。
(2)该NaOH溶液中NaOH的物质的量浓度为
________________________________________________________________________,
该NaOH溶液中由水电离出的[OH-]为__________。
(3)给该NaOH溶液加热,pH________(填“变大”、“变小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
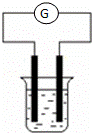
现有A、B、C、D和Cu五种金属片,将其分别用导线连接后浸入稀硫酸中(如图),每次实验时,通过灵敏电流计测出电子流动方向如下:
| G 实验分组 | 所用金属 | 电子流向 |
| ① | A、Cu | A→Cu |
| ② | C、D | D→C |
| ③ | A、C | C→A |
| ④ | B、Cu | Cu→B |
| ⑤ | … | … |
根据上述情况,回答下列问题:
(1)上述五种金属的活动性顺序是 .
(2)在①中,Cu片上观察到的现象是: ;
(3)在②中,溶液中H+向金属片 移动;
(4)在④中,两金属片上均无气泡放出.此时两金属片上的电极反应式分别为:Cu: ;B: ;
(5)如果实验⑤用B、D,则导线中电流方向为: (填B→D或D→B);
(6)已知反应:Cu+2Fe3+═Cu2++2Fe2+.请用下列试剂和材料,用上图所示装置,将此反应设计成原电池并检验正极产物.
试剂:CuCl2溶液、FeCl3溶液、FeCl2溶液、KSCN溶液、K3[Fe(CN)6]溶液、双氧水、NaOH溶液
材料:Cu片、Fe片、石墨棒
a、设计电池应选用的试剂和材料是: ;
b、检验正极产物选用的试剂是 ,检验反应的离子方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com