
 2NH3£¬£¬Ę½ŗāŗ󣬲āµĆ·“Ó¦·Å³öµÄČČĮæĪŖ18.4kJ£¬»ģŗĻĘųĢå×ܵÄĪļÖŹµÄĮæĪŖ3.6mol£¬ČŻĘ÷ÄŚµÄŃ¹Ēæ±äĪŖŌĄ“µÄ90%£®ÓÖÖŖN2ŗĶH2µÄ×Ŗ»ÆĀŹĻąĶ¬£®
2NH3£¬£¬Ę½ŗāŗ󣬲āµĆ·“Ó¦·Å³öµÄČČĮæĪŖ18.4kJ£¬»ģŗĻĘųĢå×ܵÄĪļÖŹµÄĮæĪŖ3.6mol£¬ČŻĘ÷ÄŚµÄŃ¹Ēæ±äĪŖŌĄ“µÄ90%£®ÓÖÖŖN2ŗĶH2µÄ×Ŗ»ÆĀŹĻąĶ¬£® 2NH3£¬
2NH3£¬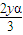 £¬ĖłŅŌy=3x£¬»Æѧ·“Ó¦Ē°ŗó£¬ĘųĢåµÄŃ¹ĒæÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±Č£¬ĖłŅŌ
£¬ĖłŅŌy=3x£¬»Æѧ·“Ó¦Ē°ŗó£¬ĘųĢåµÄŃ¹ĒæÖ®±ČµČÓŚĪļÖŹµÄĮæÖ®±Č£¬ĖłŅŌ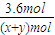 =0.9£¬¼“ x+y=4£¬¹Źx=1£¬y=3£¬
=0.9£¬¼“ x+y=4£¬¹Źx=1£¬y=3£¬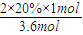 ×100%=
×100%= £¬¹Ź“š°øĪŖ£ŗ1£»3£»
£¬¹Ź“š°øĪŖ£ŗ1£»3£» £»
£»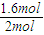 ×92 kJ?mol-1×
×92 kJ?mol-1× =73.6 kJ£¬¹Ź“š°øĪŖ£ŗ73.6£»0”Üc£¼0.4£®
=73.6 kJ£¬¹Ź“š°øĪŖ£ŗ73.6£»0”Üc£¼0.4£®


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
 2NH3£¬£¬Ę½ŗāŗ󣬲āµĆ·“Ó¦·Å³öµÄČČĮæĪŖ18.4kJ£¬»ģŗĻĘųĢå×ܵÄĪļÖŹµÄĮæĪŖ3.6mol£¬ČŻĘ÷ÄŚµÄŃ¹Ēæ±äĪŖŌĄ“µÄ90%£®ÓÖÖŖN2ŗĶH2µÄ×Ŗ»ÆĀŹĻąĶ¬£®
2NH3£¬£¬Ę½ŗāŗ󣬲āµĆ·“Ó¦·Å³öµÄČČĮæĪŖ18.4kJ£¬»ģŗĻĘųĢå×ܵÄĪļÖŹµÄĮæĪŖ3.6mol£¬ČŻĘ÷ÄŚµÄŃ¹Ēæ±äĪŖŌĄ“µÄ90%£®ÓÖÖŖN2ŗĶH2µÄ×Ŗ»ÆĀŹĻąĶ¬£®| 1 |
| 9 |
| 1 |
| 9 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| A”¢·“ӦȯĘ÷ÖŠŃ¹Ēæ²»Ėꏱ¼ä±ä»Æ¶ų±ä»Æ | B”¢»ģŗĻĘųĢåŃÕÉ«±£³Ö²»±ä | C”¢»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä | D”¢ø÷ĪļÖŹµÄĪļÖŹµÄĮæÅØ¶Č±£³Ö²»±ä |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com