
| A. | 线型结构的高分子材料分子间是靠分子间作用力紧密结合的,所以它的强度一定小 | |
| B. | 从实验测得的某高分子化合物的相对分子质量和小分子的相对分子质量含义不同 | |
| C. | 硫化橡胶为体型网状结构 | |
| D. | 线型结构的高分子,可带支链,也可不带支链 |
分析 A.线型结构的高分子,许多链节聚集在一起时,相互间的缠绕使得许多分子间接触的地方以分子间作用力紧密结合,使高分子材料的强度大大增加;
B.高分子的相对分子质量是平均相对分子质量;
C.硫化橡胶具有体型网状结构;
D.线型高分子可能含有支链.
解答 解:A.线型结构的高分子,许多链节聚集在一起时,相互间的缠绕使得许多分子间接触的地方以分子间作用力紧密结合,使高分子材料的强度大大增加,相对分子质量越大,分子间作用力就越强,故A错误;
B.高分子的相对分子质量是平均相对分子质量,而小分子的相对分子质量是确定的,故B正确;
C.硫化橡胶具有体型网状结构,有较高的强度和化学稳定性,故C正确;
D.线型高分子可能含有支链,也可能不含支链,故D正确.
故选A.
点评 本题考查了高分子化合物,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4L SO3的分子数为1NA | |
| B. | 3.9g Na2O2固体中阴离子的数目为0.1NA | |
| C. | 1mol Cl2与1mol Fe反应,转移的电子数为2NA | |
| D. | 0.1molN2和C18O含有的中子数均为1.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
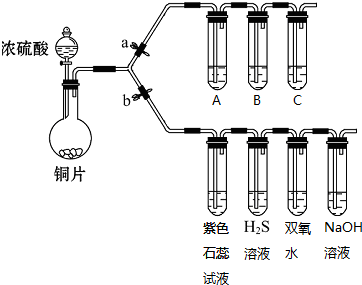
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将铁屑、溴水、苯混合制溴苯 | |
| B. | 在苯中滴入浓硝酸制硝基苯 | |
| C. | 用乙醇和乙酸混合共热制取乙酸乙酯 | |
| D. | 将铜丝在酒精灯加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
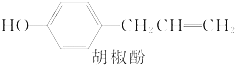
| A. | 该化合物属于芳香烃 | |
| B. | 该化合物的分子式是 C9H11O | |
| C. | 分子中所有碳原子一定处于同一平面 | |
| D. | 1 mol该化合物最多可与4 mol H2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C、S、N所形成的氧化物均为酸性氧化物 | |
| B. | “水滴石穿”是因为CaCO3与CO2、水发生了化学反应 | |
| C. | 常用作水处理剂的KAl(SO4)2和漂白粉都是强电解质 | |
| D. | 232Th 转变成233U是化学变化,233U和235U的化学性质几乎相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,向含AgCl固体的AgCl溶液中加入NaCl固体,AgCl沉淀的量不变 | |
| B. | 滴定终点时,溶液中CrO42-的浓度约为3.6×10-3 mol•L-1 | |
| C. | 向0.1moL/L AgNO3溶液中滴加3-5滴0.1moL/L NaCl溶液生成AgCl沉淀,再滴加KI溶液,生成AgI沉淀,能够说明Ksp(AgI)<Ksp(AgCl) | |
| D. | 可用0.1 mol•L-1的KI溶液代替K2CrO4做指示剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com